Professional Documents
Culture Documents
Kekuatan Medan Ligan Bundelan Fix
Uploaded by
Febrina Tri NarantiCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Kekuatan Medan Ligan Bundelan Fix
Uploaded by
Febrina Tri NarantiCopyright:
Available Formats
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
KEKUATAN MEDAN LIGAN
I. TUJUAN Mempelajari perbedaan kekuatan medan antara ligan amonia dan air II. TEORI Ion unsur transisi dapat mengikat ion-ion atau molekul netral yang memiliki pasangan elektron bebas (ligan) dengan ikatan kovalen koordinasi yang membentuk ion kompleks. Ion kompleks adalah gabungan ion (atom pusat) dengan ion lain (ligan) membentuk ion baru atau gabungan ion dengan molekul netral membentuk ion baru. Berdasarkan ligan yang diikat oleh atom pusat dalam ion kompleks, maka ada 2 macam ion kompleks : a. Ion kompleks positif Terbentuk apabila ion logam transisi (atom pusat) berikatan dengan ligan yang merupakan molekul netral seperti kompleks yang terbentuk bermuatan positif. b. Ion kompleks negatif Terbentuk apabila ion atom pusat berikatan dengan ligan yang merupakan ion negatif. Bila pada ion kompleks diberikan energi dalam bentuk cahaya, maka elektron pada orbital yang lebih rendah energinya dapat tereksitasi ke orbital yang lebih tinggi energinya. Dengan menyerap cahaya yang energinya sama dengan harga gelombangnya. Cahaya tampak terdiri dari cahaya radiasi dengan yaitu 400 -700 nm. Suatu larutan/zat padat memiliki warna tertentu karena menyerap sebagian dari komponen sinar tampak. Makin kecil maka makin kuat ikatan antara ion pusat dan ligan. Urutan kekuatan ligan sebagai berikut : CO ~ CN- NO2 dipy en NH3 ~ py NCS- H2O HCO2- OH- F- Cl- Br. Makin kecil energinya maka makin besar panjang atau sehingga ion
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
Ditinjau dari muatan ligannnya, maka ion logam dengan muatan yang lebih besar akan menghasilkan harga yang lebih besar pula karena lebih untuk Fe(NH3)64+
mudah mempolarisasikan elektron yang terdapat dalam ligan. Ukuran dari muatan logamnya mempengaruhi harga lebih besar daripada harga makin besar harga . misalnya harga untuk Nb(NH3)64+ makin besar ukuran ion maka
Menurut teori medan kristal atau crystal field theory (CFT), ikatan antara logam pusat dan ligan dalam kompleks berupa ikatan ion sehingga gaya-gaya yang ada hanya berupa gaya elektrostatik. Ion kompleks tersusun dari ion pusat yang dikelilingi oleh ion-ion lawan atau molekul-molekul yang mempunyai momen dipol permanen. Medan listrik dari ion pusat akan mempengaruhi ligan-ligan
disekelilingnya. Sedangkan medan gabungan dari ligan-ligan akan mempengaruhi elektron dari ion pusat. Pengaruh ligan tergantung pada jenisnya, terutama pada kekuatan medan listrik dan kedudukan geometris ligan dalam kompleks. Didalam ion bebas, kelima orbital d bersifat degenerete, artinya mempunyai energi yang sama dan elektron dalam orbital ini memenuhi hukum multiplycity yang maksimal. Teori medan ligan membicarakan pengaruh ligan yang tersusun secara berbeda disekitar ion pusat terhadap energi dari orbital d. Orbital d dibagi menjadi dua golongan yaitu orbital eg dan t 2g. Dengan adanya ligan disekitar ion pusat, obital d tidak lagi degenerate. Orbital d terbagi menjadi beberapa orbital dengan energi berbeda. Dikatakan juga orbital d ini mengalami splitting. Ligan didalam ion kompleks berupa ion negatif seperti F- dan CN- atau berupa molekul polar dengan muatan negatifnya mengarah pada ion pusat seperti pada H2O atau NH3. Ligan ini akan menimbulkan medan listrik yang akan menolak elektron d dari ion pusat. Karena elektron d ini terdapat diorbital paling luar dari ion pusat. Penolakkan ini menyebabkan energi level orbital d dari ion pusat bertambah.
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
Bila kelima orbital d sama dan medan ligan mempengaruhi kelimanya dengan cara yang sama, maka kelima orbital d ini akan tetap degenerate pada energi level yang lebih tinggi. Kenyataannya kelima orbital d ini tidak sama. Ada orbital eg dan t2g. Medan ligan tergantung dari letaknya disekitar ion pusat artinya apakah strukturnya oktahedral, tetrahedral atau planar segi empat. Akibat dari orbital d diurai oleh medan ligan, peristiwa ini disebut uraian medan kristal atau criystal field splitting. Uraian ini dalam medan oktahedral terlihat pada gambar dibawah ini :
eg
O t2g
a b c
Keterangan : a. Orbital d yang degenarate pada ion bebas b. Kompleks hipotesis dengan orbital d yang degenerate c. Crystal Field Splitting dalam medan oktahedral Ligan dapat diklasifikasikan atas dasar banyaknya titik-lekat kepada ion logam, yaitu : 1. Ligan monodentat yaitu ligan itu terikat pada ion logam hanya pada satu titik oleh penyumbangan satu pasangan elektron bebas kepada logam. Contoh ligan monodentat yaitu ion-ion halida, H2O atau NH3. 2. Ligan bidentat Bila molekul atau ion ligan mempunyai dua atom yang masing-masing mempunyai satu pasangan elektron bebas, maka molekul itu mempunyai
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
dua atom penyumbang, dan bisa membentuk dua ikatan koordinasi dengan ion logam yang sama. Ligan seperti ini disebut ligan bidentat. 3. Ligan multidentat Yaitu ligan yang mengandung lebih dari dua atom koordinasi per molekul, misalnya asam etilenadiaminatetraasetat (EDTA) yang mempunyai dua atom nitrogen penyumbang dan empat atom oksigen penyumbang dalam molekul, dapat merupakan heksadentat. Kestabilan suatu kompleks akan berhubungan dengan : 1. Kemampuan mengkompleks logam-logam a. Kation dengan konfigurasi gas mulia. Logam-logam alkali, alkali tanah, dan alumunium termasuk dalam grup ini. Gaya elektrostatik dominan dalam pembentukan kompleks, sehingga interaksi antara ion-ion kecil yang bermuatan tinggi, istimewa kuatnya, dan menimbulkan komplekskompleks yang stabil. b. Kation dengan sub-kulit d yang terisi lengkap c. Ion-ion logam transisi dengan sub-kulit d yang tak lengkap. 2. Ciri-ciri khas ligan Di antara ciri-ciri khas ligan yang mempengaruhi kestabilan kompleks adalah : a. Kekuatan basa dari ligan itu b. Efek khelat c. Efek-efek sterik (ruang)
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
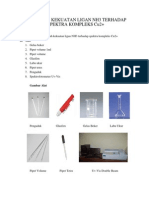
III. PROSEDUR PERCOBAAN 3.1 ALAT DAN BAHAN No 1 2 3 4 5 Alat Labu ukur 10 ml Pipet gondok 2 ml, t ml dan 10 ml Beaker glass 100 ml dan 250 ml Alat-alat gelas lain Spektrofotometer Fungsi Tempat pengenceran Pemipet larutan / zat Tempat zat Alat bantu selama pratikum Pengukur absorban
No 1 2 3 4
Bahan Larutan Ammonia 1 M Larutan ion Cu+2 0,1 M Etilendiamin 1 M Aquadest
Fungsi Sebagai ligan / zat uji Sumbar atom pusat Sebagai ligan / zat uji Sebagai pelarut
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
3.2 CARA KERJA 1. Siapkan 5 buah labu ukur 10 mL untuk memebuat larutan Cu2+ 0,02 M dalam pelarut air; 50 : 50 campuran air dan amonia dan larutan ammonia 1 M ; 75 : 25 campuran air dan larutan ammonia. 2. Larutan ion Cu2+ 0,02 M dalam larutan air dibuat dengan memindahkan 2,0 mL larutan Cu2+ 0,1 M kedalam labu ukur 10 mL dab diencerkan dengan air sampai batas. 3. Larutan ion Cu2+ 0,02 M dalam 50 : 50 campuran air dan ammonia dibuat dengan memindahlan 2,0 mL larutan Cu2+ 0,1 M kedalam albu ukur 10 mL dan diencerkan dengan 5,0 mL larutan ammonia dan kemudian dilanjutkan dengan air sampai batas. 4. Larutan ion Cu2+ 0,02 M dalam 75 : 25 campuran air dan larutan ammonia dibuat dengan memindahlan 2,0mL larutan Cu2+ 0,1 M kedalam albu ukur 10mL dan diencerkan dengan 2,5 mL larutan ammonia dan kemudian dilanjutkan dengan air sampai batas. 5. Amati serapan ketiga larutan tersebut menggunakan spektrofotometer dengan air sebagai blankonya pada panjang gelombang 510 nm 700 nm dengan interval 10 nm 6. 7. Lakukan hal yang sama pada logan etilen diamin Perbedaan kekuatan ligan antara air, dan amonia dapat diketahui dengan mebandingkan panjang gelombang maksimumnya.
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
3.3 SKEMA KERJA
Larutan Cu+2 0,02 M Dimasukkan 2 ml masing-masingnya ke 5 labu ukur 10 ml Labu 1 + air hingga 10 ml Labu 2 + 5 ml ammonia + air hingga 10 ml Labu 3 + 2,5 ml ammonia + air hingga 10 ml Labu 4 + 5 ml etilendiamin + air hingga 10 ml Labu 5 + 2,5 ml etilendiamin + air hingga 10 ml
Cu+2 dengan air 4.
Cu+2 dengan air : ammonia ( 50 : 50)
Cu+2 dengan air : ammonia (75 : 25)
Cu+2 dengan air : etilendiamin (50 : 50)
Cu+2 dengan air : etilendiamin (75 : 25)
Diukur serapan (510 700)nm dengan interval 10nm
Hasil Absorban
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
4.1 SKEMA ALAT Labu ukur 10 ml (2 ml Cu2+ 0,1 M + air)
Labu ukur 10 ml (2 ml Cu2+ 0,1 M + air dan amonia 50 : 50)
Labu ukur 10 ml (2 ml Cu2+ 0,1 M + air dan amonia 75 : 25)
Labu ukur 10 ml (2 ml Cu2+ 0,1 M + air dan etilendiamin 50 : 50)
Labu ukur 10 ml (2 ml Cu2+ 0,1 M + air dan etilendiamin 75 : 25)
Alat spektrofotometri
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
IV. DATA DAN PERHITUNGAN 4.1 DATA
510 520 530 540 550 560 570 580 590 600 610 620 630 640 650 660 670 680 690 700
Cu2+ 0,02 M 0,024 0,025 0,025 0,023 0,023 0,024 0,023 0,025 0,029 0,032 0,037 0,044 0,053 0,063 0,032 0,085 0,097 0,113 0,132 0,146
Cu2+ : NH4OH 50:50 0,39 0,493 0,594 0,692 0,776 0,858 0,925 0,973 1,002 1,013 1,009 0,989 0,926 0,886 0,837 0,792 0,74 0,723 0,684 0,632
Cu2+ : NH4OH 75 : 25 0,338 0,426 0,515 0,601 0,676 0,751 0,812 0,857 0,885 0,897 0,896 0,879 0,857 0,827 0,792 0,748 0,713 0,664 0,615 0,569
Cu2+ : en 50:50 0,982 1,112 1,202 1,256 1,273 1,257 1,213 1,147 1,068 0,986 0,896 0,798 0,712 0,63 0,558 0,487 0,434 0,384 0,334 0,293
Cu2+ : en 75 : 25 0,979 1,111 1,198 1,259 1,264 1,244 1,196 1,126 1,044 0,958 0,868 0,768 0,683 0,6 0,529 0,459 0,407 0,354 0,306 0,266
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
4.2 PERHITUNGAN 1. NH4OH 1 M M = = = 6,5 M Volume NH4OH yang yang di butuhkan untuk pengenceran dalam labu ukur 50 mL V1 x M1 V1 x 6,5 M V1 = V2 x M 2 = 50 mL x 1 M = 7,7 mL
2. Etilen diamin 1 M M = = = 14, 9 M Volume etilen diamin yang di butuhkan untuk pengenceran dalam labu ukur 50 mL V1 x M1 V1 x 14, 9 M V1 3. CuSO4.5H2O M = = V2 x M 2 = 50 mL x 1 M = 3,33 mL Cu2+ 0,1 M
x x
0,1 M = gram = 1,2484 M 4. Penentuan energi E=
h = 6,626 x 10-34 Js c = 3 x 108 m/s
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
a. Untuk Cu2+ E =
max = 700 nm
= 2,839 x 10-19 Js b. Untuk Cu2+ + larutan NH4OH (50 : 50) E max = 600 nm
=
= 3,313 x 10-19 Js
c. Untuk Cu2+ + larutan NH4OH (75 : 25) E = = 3,313 x 10-19 Js d. Untuk Cu2+ + larutan etilen diamin (50 : 50) E = = 3,614 x 10-19 Js e. Untuk Cu2+ + larutan etilen diamin (75 : 25) E = = 3,614 x 10-19 Js Kekuatan medan ligan en > NH3> H2O
max = 600 nm
max = 550 nm
max = 550 nm
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
GRAFIK
1. Untuk larutan Cu2+ 0,02 M
Panjang gelombang Vs Adsorban
0.16 0.14 0.12 Adsorban 0.1 0.08 0.06 0.04 0.02 0 510520530540550560570580590600610620630640650660670680690700 Panjang gelombang
2. Untuk larutan Cu2+ + lar. NH4OH (50 : 50)
Panjang gelombang Vs Adsorban
1.2 1 Adsorban 0.8 0.6 0.4 0.2 0 510520530540550560570580590600610620630640650660670680690700 Panjang gelombang
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
3. Untuk larutan Cu2+ + lar. NH4OH (75 : 25)
Panjang gelombang Vs Adsorban
3.5 3 2.5 2 1.5 1 0.5 0 510 520 530 540 550 560 570 580 590 600 610 620 630 640 650 660 670 680 680 690 690 Panjang gelombang 700 700 Adsorban
4. Untuk larutan Cu2+ + lar. etilen diamin (50 : 50)
Panjang gelombang Vs Adsorban
1.4 1.2 1 0.8 0.6 0.4 0.2 0 510 520 530 540 550 560 570 580 590 600 610 620 630 640 650 660 Panjang gelombang 670 Adsorban
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
5. Untuk larutan Cu2+ + lar. etilen diamin (75 : 25)
Panjang gelombang Vs Adsorban
1.4 1.2 1 0.8 0.6 0.4 0.2 0 510 520 530 540 550 560 570 580 590 600 610 620 630 640 650 660 670 680 690 700 Panjang gelombang
Adsorban
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
V. PENGAMATAN DAN PEMBAHASAN 5.1 PENGAMATAN a. PENGAMATAN SETIAP LANGKAH KERJA No 1. LANGKAH KERJA DAN REAKSI disiapkan 4 buah labu ukur 10mL masing masing di isi dengan 2 mL larutan Cu2+ 0,1 M FOTO PENGAMATAN Larutan Cu2+ 0,1 M berwarna biru muda. ANALISIS Larutan berwarna biru muda ini dieroleh dari pengenceran larutan Cu2+ yang sebelumnya berwarna biru.
Pada labu 1 dan 2 masing masing ditambahkan 2,5 mL dan 5mL ammonia.
Campuran Larutan Cu2+ 0,1 M dan ammonia memberikan warna biru tua.
Warna larutan disebabkan karena adanya spiling pada orbital d atom pusat.
Pada labu 3 dan 4 masingmasing diisi dengan 2,5 mL dan 5 mL etilendiamin..
Campuran Larutan Cu2+ 0,1 M dan etielndiamin memberikan warna biru keunguan
Warna larutan disebabkan karena adanya spiling pada orbital d atom pusat.
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
4 buah larutan yang telah di sipakan, diencerkan dengan aquadest sampai tanda batas.
Ligan yang berbeda akan memebrikan warna kompleks yang berbeda.
Karena ligan yang di gunakan berbeda, maka campuran memberikan warna yang berbeda.
Amati serapan larutan yang telah disiapkan dengan menggunakan spektrofotometer.
Pengukuran serapan bertujuan untuk mengetahui panjang gelombang maksimum nya, untuk membandingkan perbedaan kekuatan ligan
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
b. No 1
PENGAMATAN SIFAT FISIK RENDEMEN HASIL AKHIR SENYAWA DAN STRUKTUR KIMIA PRODUK Cu(H2O)62+ STRUKTUR GEOMETRI DAN HIBRIDISASI
29Cu
ANALISIS Kompleks Cu(H2O)62+ Berwarna biru muda, kompleks ini berwarna karena adanya orbital d yang tidak terisi penuh. Struktur geometri dari kompleks ini yaitu oktahedral dengan hibridisasi sp3d2.
2+
= (Ar)18 4s2 3d9
Cu 2+= (Ar)18 4s0 3d9
.. .. .. .. .. ..
3d
4s
4p
4d
Hibridisasi = sp3d2 ( oktahedral) Cu(NH3)62+
2+
29Cu
= (Ar)18 4s2 3d9
Cu 2+= (Ar)18 4s0 3d9
.. .. .. .. .. ..
3d
4s
4p
4d
Hibridisasi = sp3d2 ( oktahedral)
Kompleks Cu(NH3)62+ Berwarna biru tua, karena warna kompleks levih tua dari yang pertama, akibatnya absorban maksimumnya terletak pada panjang gelombang yang lebih pendek dari yna pertama Struktur geometri dari kompleks ini yaitu
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
Cu(en)32+
2+
29Cu
= (Ar)18 4s2 3d9
Cu 2+= (Ar)18 4s0 3d9
.. .. .. .. .. ..
3d
4s
4p
4d
Hibridisasi = sp3d2 ( oktahedral)
oktahedral dengan hibridisasi sp3d2. Kompleks Cu(en)32+ Berwarna biru keunguan, dan warna kompleks levih tua dari yang sebelumnya, akibatnya absorban maksimumnya terletak pada panjang gelombang yang lebih pendek dari yang sebelumnya. Struktur geometri dari kompleks ini yaitu oktahedral dengan hibridisasi sp3d2.
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
5.2 PEMBAHASAN Pada praktikum kimia anorganik II kali ini, percobaan yang kami lakukan yaitu mengukur kekuatan medan ligan antara air,amonia dan etieln diamin. Dimana sebagai atom pusatnya adalah Cu2+. Senyawa kompleks merupakan senyawa yang berwarna , hal ini terjadi karena atom pusat yang memiliki orbital d yang tidak penuh, akibatnya orbital d ini akan terspiliting oleh ligan dengan energi sebesar 10Dq. Energi yang terspliting itu nantinya yang akan memancarkan warna. Warna yang berbedabeda pada senyawa kompleks tergantung pada beberapa besarnya energi 10 Dq. Untuk menentukan kekuatan ligan-ligan antara air, ammonia dan etilen diamin, dilakukan pengukuran absorban masing-masing larutan pada panjang gelombang 510 nm 700 nm. Dari pengukuran didapatkan panjang gelombang dengan serapan terbesar terdapat pada air yaitu pada 700nm, sedangkan pada amonia pada 600 nm dan etilen diamin pada 550 nm. Dari data terlihat bahwa, meskipun perbandingan komposisi pada masing masing campuran amonia atupun etilen diamin berbeda, serapan maksimum tetap berada pada panjang gelombang yang sama. Hal ini karena serapan maksimum tidak di pengaruhi oleh komposisi tapi dipengaruhi oleh ligan yang terikat. Warna larutan juga berpengaruhh pada pengukuran nilai absorban, dari pengamatan terlihat bahwa warna larutan yang lebih terang akan membrikan absorban pada panjang gelombang yang lebih tinggi, dan sebaliknya. Hal ini karena semakin tua warna larutan artinya partikel yang menyerap sinar semakin banyak,dan berarti panjang gelombang akan semakin pendek. Pada praktkium ini karena warna larutan air lebih terang di banding ammonia, dan ammonia lebih terang dibanding etilendiamin ( air : ammonia : etilendiamin = biru muda : biru tua ; biru keunguan ), maka serapan maksimumn air juga berada pada panjang gelombang yang lebih besar dari pada amonia dan ammonia lebih besar di banding etilendiamin.
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
Dari panjang gelombang
maksimum yang telah diketahui, kita dapat
menghitung energi, dari perhitungan terlihat bahwa semakin kecil panjang gelombang masimum, maka energi yang dibutuhkan semakin kecil, dan energi berbanding lurus dengan kekuatan ligan . artinya semakin besar energi maka kekuatan medan ligan semakin besar. Karena Eair < E amonia < E etilendiamin, maka kekuatan medan ligan Air < Ammonia < Etilen diamin.
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
VI. KESIMPULAN DAN SARAN 6.1 Kesimpulan Dari percobaan yang telah kami lakukan dapat diambil kesimpulan, yaitu : a. Kompleks Cu dengan etilen diamin lebih stabil dibandingkan dengan kompleks Cu dengan ammonia ataupun kompleks Cu dengan air b. Urutan kekuatan ligan : Air < Ammonia < Etilen diamin c. Semakin besar nilai E, kompleks semakin stabil d. Warna pada senyawa kompleks diakibatkan oleh pemancaran energi orbital d yang terspliting 6.2 Saran Agar praktikan selanjutnya mendapatkan hasil yang lebih baik,maka disarankan untuk : a. Hati-hati dan teliti dalam pengenceran larutan b. Hati-hati dan teliti dalam pengukuran absorban dengan
spektrofotometer c. Pahami cara kerja dengan baik d. Pastikan kuvet yang digunakan benar-benar bersih
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
VII. TUGAS PRA PRAKTIKUM 1. Urutan kekuatan medan ligan berdasarkan deret spektro yaitu : Jawab : CO ~ CN- NO2 dipy en NH3 ~ py NCS- H2O HCO2- OH- F- Cl- BrFaktor yang mempengaruhi harga energi pembelahan medan kristal yaitu : Jawab : a. Keadaan oksidasi ion logam, perbedaan energi akan bertambah besar dengan bertambahnya biloks kation b. Sifat aliansi ion logam c. JumLah bentuk ligan 3. Kenapa teori medan kristal dapat menjelaskan tentang warna pada senyawa kompleks? Jawab: Karena terjadinya spliting pada orbital d yang menyebabkan elektron tereksitasi, saat elektron tereksitasi dan kembali kekeadaan dasar, saat itulah elektron akan memancarkan cahaya.
2.
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
VIII. JURNAL 8.1 ANALISIS a. Skema kerja (NH4)2S04.ZnS04 6H20 , (NH4hS04 NiS04.6H20 dan (NH4)2S04.MnS0 .6H40 Dipanaskan pada beberapa temperatur dengan bebmacam interval waktu Pemanasan dilakukan pada tekanan I X 10-4 torr Kristal garam dengan Kadar hidrat rendah Dibuat kurva persentase air masing-masing garam.
b. Analisis metoda yang dipakai Pada jurnal ini, metoda yang di gunakan dalam menentukan medan ligan adalah metoda termokimia, dimana hal yang berperan disini yaitu interval suhu yang bervariasi yang di gunakan untuk pemanasan hidrat ,dari suhu inilah akan di peroleh energi yang nantinya akan di buat kurva untuk mengetahui energi spliting masing masing kompleks. c. Analisis hasil yang didapatkan Pada jurnal hasil yang diperoleh yaitu energi 10Dq pada masing masing garam kompleks yang di gunakan,dari energi yang didapatkan maka kita dapat mengetahui perbedaan energi 10Dq pada masing masing garam kompleks yang di gunakan. d. Kelebihan metoda jurnal di banding praktikum Dari metoda yang digunakan pada jurnal kita dapat mengetahui perbedaan energi 10Dq pada masing masing garam kompleks yang di gunakan. Sedang kan pada praktikum yang di hitung adalah kekuatan medan logan dari perbedaan energi masing masing ligan.
OBJEK II - KEKUATAN MEDAN LIGAN
PRAKTIKUM KIMIA ANORGANIK II SEMESTER GANJIL TAHUN AJARAN 2012/2013
IX. DAFTAR PUSTAKA Cotton, Wilkingston. 1989. KIMIA ANORGANIK DASAR. UI : Jakarta Fetrucci, Ralph. 1992. KIMIA DASAR PRINSIP DAN TERAPAN MODERN. Erlangga : Jakarta. Soekardjo. 1989. KIMIA FISIKA. Bina Aksara : Jakarta Underwood. 1990. ANALISA KIMIA KUANTITATIF. Jakarta : Erlangga.
OBJEK II - KEKUATAN MEDAN LIGAN
You might also like
- Kekuatan Medan LiganDocument12 pagesKekuatan Medan LiganDamon NealNo ratings yet
- Percobaan I - Kekuatan Medan LiganDocument17 pagesPercobaan I - Kekuatan Medan LiganlyraNo ratings yet
- Fotometri 1 UnpadDocument7 pagesFotometri 1 UnpadIlham maulanaNo ratings yet
- ZAT PADATDocument16 pagesZAT PADATMarinda Mayliansarisyah PutriNo ratings yet
- Percobaan II Spektrum UV-VISDocument26 pagesPercobaan II Spektrum UV-VISsatrianiNo ratings yet
- Pembuatan Kalium NitratDocument10 pagesPembuatan Kalium NitratDila Rizci Lee0% (1)
- Pembuatan Kalium Aluminium Sulfat2Document9 pagesPembuatan Kalium Aluminium Sulfat2Muhammad Syarif HidayatullahNo ratings yet
- PEMBUATAN DAN REAKSI SENYAWA KOMPLEKS (40Document5 pagesPEMBUATAN DAN REAKSI SENYAWA KOMPLEKS (40Amanda PujiastutiNo ratings yet
- UNSUR ALKALI TANAH (Sri Rizka Fadila Guci)Document17 pagesUNSUR ALKALI TANAH (Sri Rizka Fadila Guci)Dila Rizci LeeNo ratings yet
- TEORIMEDANKRISTALDocument2 pagesTEORIMEDANKRISTALike ramdaniyahNo ratings yet
- OPTIMALKAN LIGANDocument27 pagesOPTIMALKAN LIGANNurhasfah SyawaliahNo ratings yet
- Ujian Tengah Semester: Evaluasi 1Document13 pagesUjian Tengah Semester: Evaluasi 1Jihan AudiraNo ratings yet
- PENETAPAN BESIDocument10 pagesPENETAPAN BESIniaNo ratings yet
- Makalah Coloumetri Dan ElektrogravimetriDocument15 pagesMakalah Coloumetri Dan ElektrogravimetriTafta Na E'i100% (1)
- Pembuatan Garam Kompleks Dan Garam RangkapDocument14 pagesPembuatan Garam Kompleks Dan Garam RangkapAnggia Putri Gustami0% (1)
- Logam Transisi KimiaDocument50 pagesLogam Transisi KimiaRama AgnestiarawanNo ratings yet
- Jawaban PertanyaaanDocument6 pagesJawaban PertanyaaanChris TyasihNo ratings yet
- Laporan Pengaruh Kekuatan Ligan Nh3 Terhadap Spektra Kompleks Cu2Document10 pagesLaporan Pengaruh Kekuatan Ligan Nh3 Terhadap Spektra Kompleks Cu2Anggia Putri Gustami50% (2)
- RetaDocument9 pagesRetaYeni Mareta Dwi RakhmadaNo ratings yet
- Percobaan 3 Penetapan Konsentrasi Sulfat Didalam Larutan K2SO4 Secara Turbidimetri Dengan Alat Spektronik 20Document16 pagesPercobaan 3 Penetapan Konsentrasi Sulfat Didalam Larutan K2SO4 Secara Turbidimetri Dengan Alat Spektronik 20SitiNurAzizah A.TNo ratings yet
- PEMBUATAN KROM ALUM FixDocument11 pagesPEMBUATAN KROM ALUM FixFielda Ayu Amasfa100% (1)
- Lapleng KonduktometriDocument14 pagesLapleng KonduktometriIra SepriyaniNo ratings yet
- Makalah Bab Disosiasi Dan Substitusi LiganDocument17 pagesMakalah Bab Disosiasi Dan Substitusi LiganRifki SolihatunNo ratings yet
- Kromatografi Penukar IonDocument12 pagesKromatografi Penukar IonAgustina ItinNo ratings yet
- REAKSI REDOKSDocument47 pagesREAKSI REDOKSKamilPrislaOnyxNo ratings yet
- Pelarut Bukan AirDocument29 pagesPelarut Bukan AirJoseph Ricky DamaraNo ratings yet
- Kekuatan Medan LiganDocument27 pagesKekuatan Medan LiganMegaNo ratings yet
- Laporan AnorganikkuDocument15 pagesLaporan AnorganikkuArrumJessi0% (1)
- FAC-MERDocument25 pagesFAC-MERHamdan Nurul FikriNo ratings yet
- Laporan Praktikum Kimfis Pengukuran Viskositas Cairan Untuk Menentukan Jari-JarimolekulDocument14 pagesLaporan Praktikum Kimfis Pengukuran Viskositas Cairan Untuk Menentukan Jari-JarimolekulPutu AstiniNo ratings yet
- Laporan Praktikum KI 3131 Kimia Unsur Golongan Utama Modul 1 Reaksi-Reaksi Kimia Senyawa Golongan UtamaDocument6 pagesLaporan Praktikum KI 3131 Kimia Unsur Golongan Utama Modul 1 Reaksi-Reaksi Kimia Senyawa Golongan Utamajessica sherryNo ratings yet
- Hukum FotokimiaDocument12 pagesHukum FotokimiaJoel Lo Amo100% (1)
- Laporan Praktikum AnorganikDocument5 pagesLaporan Praktikum AnorganikNisrina Rizkia100% (2)
- Term Simbol ElektronDocument2 pagesTerm Simbol ElektronAnnisa IndriyaniNo ratings yet
- Lapleng Edta Fiks AkterDocument18 pagesLapleng Edta Fiks AkteraktherNo ratings yet
- JUDULDocument3 pagesJUDULnilaNo ratings yet
- Rangkuman Teori Medan LiganDocument8 pagesRangkuman Teori Medan LiganShinta Novita SariNo ratings yet
- Distorsi Kompleks OktahedralDocument6 pagesDistorsi Kompleks OktahedralFirda NurfaidaNo ratings yet
- Sintesis Kristal AlumDocument5 pagesSintesis Kristal AlumFajar RizkiNo ratings yet
- LKM OksigenDocument13 pagesLKM OksigenGayatri Dewi50% (2)
- Kurva KonduktometriDocument13 pagesKurva KonduktometriDiayan WidyaNo ratings yet
- Deska Laporan Percobaan II Kristal Tunggal Kal (So4) 2Document8 pagesDeska Laporan Percobaan II Kristal Tunggal Kal (So4) 2Deska Vrayoga Fauzi Aditama II100% (2)
- Laporan Kimia (Periode 3)Document17 pagesLaporan Kimia (Periode 3)Ayu Susmhita100% (1)
- Tugas KimiaDocument3 pagesTugas KimiaNurita SariNo ratings yet
- PERCOBAAN X Penjerapan Zat Cair Pada Material Berpori FixDocument20 pagesPERCOBAAN X Penjerapan Zat Cair Pada Material Berpori Fixratna kurniawati50% (2)
- Garam Rangkap Dan Garam KompleksDocument6 pagesGaram Rangkap Dan Garam KompleksChristopher Herman100% (1)
- Kontraksi Lantanida dan PenyebabnyaDocument1 pageKontraksi Lantanida dan PenyebabnyaDhea Umi AmaliaNo ratings yet
- Kromatografi Penukar IonDocument8 pagesKromatografi Penukar IonGokil Heru50% (2)
- Bundelan Objek 5 Lengkap YuliDocument32 pagesBundelan Objek 5 Lengkap YuliCitra Ilham Maulana0% (1)
- Tetraamintembaga II SulfatDocument17 pagesTetraamintembaga II SulfatKhunaz Miligh Ci'Mommye0% (1)
- Laporan Praktikum Kimia Koordinasi Acara 2 BLM FixDocument11 pagesLaporan Praktikum Kimia Koordinasi Acara 2 BLM Fixsekar nuraniNo ratings yet
- Percobaan 2 Ikatan Kimia (Deviyanti Leo Mappa)Document16 pagesPercobaan 2 Ikatan Kimia (Deviyanti Leo Mappa)deviyantiileomappaNo ratings yet
- Kekuatan Medan LiganDocument22 pagesKekuatan Medan LiganHandayani Ingiendt DicienthandicaiankNo ratings yet
- Prinsip Elektrokimia Dasar PotensiometriDocument25 pagesPrinsip Elektrokimia Dasar PotensiometriAnonymous W6zPy3fImvNo ratings yet
- Laporan Praktikum Perc. 8 TGDocument17 pagesLaporan Praktikum Perc. 8 TGsatriasastra08No ratings yet
- Kekuatan Medan LiganDocument24 pagesKekuatan Medan LiganulfatikhahNo ratings yet
- Kekuatan Medan Ligan LaporanDocument18 pagesKekuatan Medan Ligan LaporandyahdsNo ratings yet
- Buku PotensiometriDocument185 pagesBuku PotensiometriTri SulyonoNo ratings yet
- KONDUKTIVITAS LARUTANDocument19 pagesKONDUKTIVITAS LARUTANGaluh Arya Ramdani100% (1)
- Ikatan KimiaDocument41 pagesIkatan KimiaFrna AprNo ratings yet
- Model Real TeachingDocument11 pagesModel Real TeachingFebrina Tri NarantiNo ratings yet
- Woodward FebrinaDocument13 pagesWoodward FebrinaFebrina Tri NarantiNo ratings yet
- Objek 4Document12 pagesObjek 4Miftahurrahmi MiraNo ratings yet
- Bahan An orDocument13 pagesBahan An orFebrina Tri NarantiNo ratings yet
- OPTIMASI ARGENTOMETRIDocument15 pagesOPTIMASI ARGENTOMETRIAhmed QomaruddinNo ratings yet
- Rincian Minggu Efektif Kls 8 SMTR Genap 2012-2013Document3 pagesRincian Minggu Efektif Kls 8 SMTR Genap 2012-2013Febrina Tri NarantiNo ratings yet
- Garam NaclDocument29 pagesGaram NaclFebrina Tri Naranti100% (1)
- Presentation Febrina Tri NarantiDocument3 pagesPresentation Febrina Tri NarantiFebrina Tri NarantiNo ratings yet
- Pembahasan JurnalllDocument5 pagesPembahasan JurnalllFebrina Tri NarantiNo ratings yet
- ANALISIS KUANTITATIF STRUKTUR MOLEKUL BERFLOURESENSIDocument4 pagesANALISIS KUANTITATIF STRUKTUR MOLEKUL BERFLOURESENSIFebrina Tri NarantiNo ratings yet
- Persentasi SKADocument34 pagesPersentasi SKAFebrina Tri NarantiNo ratings yet
- Woodward FebrinaDocument13 pagesWoodward FebrinaFebrina Tri NarantiNo ratings yet
- Perhitungan Kelompok SpektroDocument10 pagesPerhitungan Kelompok SpektroFebrina Tri NarantiNo ratings yet
- Presentation Febrina Tri NarantiDocument3 pagesPresentation Febrina Tri NarantiFebrina Tri NarantiNo ratings yet
- Punya Trio, Vela, AntiDocument3 pagesPunya Trio, Vela, AntiFebrina Tri NarantiNo ratings yet
- Konduktometri MakalahDocument20 pagesKonduktometri MakalahFebrina Tri NarantiNo ratings yet
- Gula ReduksiDocument29 pagesGula ReduksiFebrina Tri Naranti100% (2)
- Lan TanidaDocument44 pagesLan TanidaFebrina Tri NarantiNo ratings yet
- Bank Soal Kimfis IDocument5 pagesBank Soal Kimfis IFebrina Tri NarantiNo ratings yet
- Tegangan PermukaanDocument4 pagesTegangan Permukaananon-382588100% (4)
- Pembentukan BPUPKIDocument13 pagesPembentukan BPUPKIFebrina Tri NarantiNo ratings yet
- 07 - Rincian Minggu EfektifDocument2 pages07 - Rincian Minggu EfektifFebrina Tri NarantiNo ratings yet
- Asam Amino Dan ProteinDocument23 pagesAsam Amino Dan ProteinDestawira Hariani TaharNo ratings yet
- Tegangan PermukaanDocument4 pagesTegangan Permukaananon-382588100% (4)
- Kalor PembakaranDocument2 pagesKalor PembakaranFebrina Tri NarantiNo ratings yet
- SINTESA METIL SALISILATDocument14 pagesSINTESA METIL SALISILATFebrina Tri NarantiNo ratings yet
- Membuat Larutan Dengan Konsentrasi TertentuDocument3 pagesMembuat Larutan Dengan Konsentrasi TertentuIntan Putri RahayuNo ratings yet
- KoligatifDocument8 pagesKoligatifMuhammad Ikhsan100% (1)
- Vii. Hukum RaoultDocument5 pagesVii. Hukum RaoultFebrina Tri NarantiNo ratings yet