Professional Documents
Culture Documents
MS Testo
Uploaded by
Alessandro Del GrandeOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
MS Testo
Uploaded by
Alessandro Del GrandeCopyright:
Available Formats
2015
Spettrometria di massa (MS)
Prof. Giorgio Bonaga
Spettrometria di massa
INDICE
1. Premessa ...............................................................................
pag. 2
2. Cenni storici .........................................................................
"
3. La strumentazione MS ............................................................
3.1. Sistema del vuoto .......................................................
3.2. Sistema di introduzione del campione ....................
3.3. Ionizzazione e sorgenti ioniche ................................
3.4. Sistema di separazione degli ioni .............................
3.5. Sistema di rivelazione degli ioni ...............................
3.6. Sistema di registrazione degli ioni ............................
3.7. Potere risolvente in MS .................................................
3.8. Sensibilit strumentale in MS .....................................
"
"
"
"
"
"
"
"
"
9
10
14
17
39
55
57
58
60
4. Lo spettro di massa ..............................................................
"
62
5. Formazione e decomposizione dello ione molecolare ......
"
74
6. Interpretazione dello spettro di massa ..............................
" 100
7. Spettrometria di massa tandem (MS/MS) .........................
" 101
G. Bonaga
1. PREMESSA
La massa e le radiazioni elettromagnetiche sono le due qualit fondamentali delluniverso.
Numerosi metodi spettroscopici studiano linterazione tra le frequenze delle radiazioni
elettromagnetiche e la materia:
UV
IR
RAMAN
RAGGI X
NMR
Ultraviolet Spectroscopy
Infrared Spectroscopy
Raman Spectroscopy
X-ray Diffraction
Nuclear Magnetic Resonance
ma una sola tecnica in grado di rivelare la massa:
MS
Mass Spectrometry
La spettrometria di massa possiede alcune caratteristiche peculiari:
a) applicabile a tutti gli elementi;
b) pu analizzare sostanze di peso molecolare superiore a 300.000 a.m.u. o Da (Dalton);
c) pu rilevare singoli atomi o singole molecole;
d) fornisce una risposta quantitativamente lineare per oltre 15 ordini di grandezza (1 fg);
e) fornisce una risposta proporzionale alla concentrazione del composto analizzato.
La spettrometria di massa applicata alla chimica organica si basa sulla formazione di ioni
molecolari (o quasi-molecolari) - mediante modi di ionizzazione molto diversi in funzione
del campione da analizzare (peso molecolare e quantit del campione) - e sullo studio del
modo con cui essi si frammentano.
La ionizzazione delle molecole organiche pu produrre ioni positivi (da cui la positive-ions
mass spectrometry) o ioni negativi (da cui la negative-ions mass spectrometry), sebbene la
resa in ioni positivi sia normalmente molto maggiore di quella in ioni negativi (circa 103).
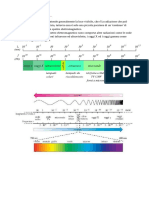
C unanalogia tra la separazione delle lunghezze donda di una radiazione luminosa e la
separazione, in base al rapporto m/z, degli ioni che si generano da una molecola ionizzata
(Fig. 1).
Un prisma lanalizzatore che separa la radiazione luminosa nelle diverse , dando origine
alla regione visibile (VIS) dello spettro elettromagnetico; lanalizzatore il settore dello
spettrometro che separa gli ioni, in base al rapporto m/z, che si formano per ionizzazione
delle molecole neutre e dalla loro frammentazione, dando origine allo spettro di massa.
Spettrometria di massa
Fig. 1 Analogia tra la separazione delle lunghezze donda e degli ioni m/z.
Lo spettro di massa (Fig. 2) un diagramma nel quale in ascissa sono riportati i diversi
valori m/z degli ioni che sono stati separati dallanalizzatore e in ordinata la loro
abbondanza relativa (ponendo uguale a 100 l'abbondanza di m/z pi intenso).
m/z
Fig. 2 Spettro di massa dellacido benzoico (mol wt 122)
G. Bonaga
2. CENNI STORICI
Nel 1880 furono rivelati i raggi catodici mediante esperienze fatte con il tubo di Geissler
(Fig. 3), un tubo che porta saldati all'interno due elettrodi collegati con un generatore di
corrente nel quale, mediante una pompa da vuoto, si pu ridurre la pressione interna.
Fig. 3 - Tubo di Geissler (1880)
In condizioni normali di pressione e di temperatura, lapplicazione di una differenza di
potenziale (d.d.p.) tra gli elettrodi produce una corrente elettrica che si manifesta con una
scintilla, dal momento che i gas presenti nel tubo sono cattivi conduttori dellelettricit.
Riducendo la pressione nel tubo a circa 10-3 torr, si ottiene la rarefazione dei gas interni ed il
passaggio di corrente elettrica - dovuto alla d.d.p. - si manifesta sottoforma di una
luminescenza dovuta ai raggi che, emessi dal catodo, si propagano con traiettoria rettilinea
verso lanodo. Questi raggi, detti appunto raggi catodici, sono particelle di carica negativa e
di massa estremamente ridotta, sempre uguali indipendentemente dal materiale usato come
catodo. Di essi Thomson, nel 1897, misur il rapporto massa/carica (= m/z) e stabil che
erano elettroni costituenti un fascio (electron beam) che veniva deviato da campi elettrici e
da campi magnetici esterni.
Nel 1886 Goldstein, modificando un tubo di Geissler (per sostituzione del catodo con un
catodo forato), individu delle particelle che attraversando il foro del catodo si
propagavano in direzione opposta a quella dei raggi catodici (Fig. 4). Goldstein osserv una
luminescenza dietro il catodo e accert che un campo magnetico deviava questo fascio in
direzione opposta a quella degli elettroni.
Fig. 4 - Tubo di Goldstein (1886)
Questi raggi, detti raggi canale, risultarono essere particelle positive la cui massa
dipendeva dal gas o dai gas contenuti nel tubo. I gas residui nel tubo, dunque, vengono
Spettrometria di massa
ionizzati per urto con i raggi catodici e costituiscono un fascio di ioni positivi (positive-ions
beam).
Nel 1913, Thomson, armonizzando i risultati ottenuti fino a quellepoca dalla fisica delle
particelle, costru il primo spettrografo di massa (Fig. 5), cio uno strumento in grado di
rivelare la massa degli ioni positivi prodotti da un gas immesso in un tubo di Geissler
modificato. Lo strumento di Thomson un tubo a catodo forato, provvisto anche di un
settore elettrostatico e di un settore magnetico i cui campi paralleli (elettrico E e magnetico
H) sono in grado di deflettere gli ioni positivi con una curvatura parabolica il cui raggio
dipende dal rapporto m/z di ciascun ione prodotto. Gli ioni vengono rivelati da una lastra
fotosensibile (fotoplacca) nella quale si manifestano le loro tracce paraboliche (Fig. 6).
Fig. 5 - Spettrografo di massa di Thomson (1913)
Immettendo nel tubo a scarica dellanidride carbonica, Thomson osserv le tracce
paraboliche corrispondenti ai seguenti ioni:
CO2+
CO+
C2+
O+
C+
m/z
m/z
m/z
m/z
m/z
44
28
24
16
12
Fig. 6 - Fotoplacca
G. Bonaga
Nel 1919, Aston modific lo spettrografo di Thomson introducendo nel tubo 3 fenditure,
lungo il cammino degli ioni positivi, in modo da ottimizzare le traiettorie degli ioni (Fig. 7).
Fig. 7 - Spettrografo di Aston (1919)
Aston separ anche il settore elettrostatico da quello magnetico, in modo da raccogliere
sulla fotoplacca dei segnali con laspetto di righe nette ed intense, anzich con laspetto
delle parabole di Thomson. Anche Aston osserv che gli ioni positivi mostravano masse
diverse da mettere in relazione con la natura del gas introdotto nello spettrografo, ma
osserv anche che lo stesso gas produceva degli ioni positivi di massa diversa. Il miglior
potere risolvente (risoluzione) dello strumento di Aston riusciva a separare gli isotopi dei
diversi atomi, con un procedimento diverso da quello che si basa sulla velocit di diffusione
delle molecole neutre (legge di Graham), cio basato soltanto sulla differenza della loro
massa. Aston, dunque, separ gli isotopi in base alla deflessione di particelle con un diverso
rapporto m/z, mediante lapplicazione di un campo magnetico e di un campo elettrico.
Introducendo lo stesso gas nel tubo di scarica, Thomson ed Aston ottenevano degli spettri di
massa (in realt delle righe) differenti, i cui aspetti possono essere descritti con 2 esempi.
1) NEON (Ne)
20
Ne
20
Ne
22
m/z
10
20 30
THOMSON
Thomson
10
Ne
20 30
ASTON
Aston
Spettrometria di massa
Con lo strumento di Thomson era individuabile un unico segnale a m/z 20, corrispondente
al nuclide 20
10 Ne , mentre con quello di Aston si osservavano due segnali, uno a m/z 20 e uno
22
a m/z 22, corrispondenti al nuclidi 20
10 Ne e 10 Ne .
Le abbondanze percentuali degli ioni a m/z 20 = 90,91% e a m/z 22 = 9,09% corrispondono
22
alla distribuzione isotopica del neon, 20
10 Ne / 10 Ne = 10/1, dalla quale si ottiene il peso atomico
del neon (20x90,91/100+22 x9,09/100 = 20,1818).
2) CLORO (Cl2)
70
70
+
Cl2
+
Cl2
72
+
Cl2
74
m/z
60
70 80
60
THOMSON
Thomson
+
Cl2
70 80
ASTON
Aston
Nel caso del cloro Thomson osservava un unico segnale a m/z 70, corrispondente allo ione
della molecola 35Cl35Cl, mentre Aston ne osservava tre, corrispondenti alle tre
combinazioni isotopiche: 35Cl35Cl (m/z = 70), 35Cl37Cl (m/z = 72) e 37Cl37Cl (m/z= 74). Il
rapporto tra le abbondanze dei picchi a m/z 70, 72 e 74 era coerente con la distribuzione
35
isotopica dei nuclidi 17
Cl/37
17 Cl = 3/1, ed il risultato del binomio:
(a + b)n
dove a e b sono le abbondanze naturali dei 2 nuclidi ed n il numero di atomi di
cloro.
Infatti:
(a + b)2 = a2 + 2ab + b2 = 9:6:1
e questi rapporti sono esattamente coincidenti con le abbondanze relative dei tre segnali
isotopici 35Cl35Cl; 35Cl 37Cl; 37Cl 37Cl.
Nel 1920 Dempster (Fig. 8) modific lo spettrografo di Aston allo scopo di eliminarne i 3
limiti principali:
1.
2.
3.
la bassa resa in ioni positivi;
la bassa velocit degli ioni positivi;
le diverse velocit degli ioni in funzione della loro massa.
Il primo limite determinava dei segnali deboli (bassa sensibilit) che venivano registrati con
difficolt, il secondo ed il terzo producevano un ion beam poco consistente e nel quale
venivano discriminati specialmente gli ioni a massa pi elevata (bassa risoluzione).
7
G. Bonaga
Fig. 8 - Spettrometro di massa di Dempster (1920)
Dempster adott un filamento al posto del catodo forato, allineato con una placca
dellanodo, e percorso da una corrente elettrica capace di produrre gli elettroni per
termoemissione. Questo electron beam costituito da elettroni a pi alta energia era in grado
di produrre una maggior resa ionica, quindi un ion beam pi intenso. Il compartimento
dello spettrografo in cui si producono gli ioni positivi a pressione estremamente ridotta la
sorgente ionica (ion source) dalla cui fenditura, normale al piano dellelectron beam,
escono gli ioni positivi.
Alluscita dalla sorgente un settore elettrostatico ad elevata d.d.p. (E, in Volts) crea un campo
di accelerazione capace di conferire agli ioni una velocit elevata. Gli ioni accelerati
entrano, attraverso una fenditura (slit), nel settore magnetico semicircolare ove, sotto
lazione di un campo magnetico (H, in Gauss), deflettono con un raggio di curvatura che
funzione del loro rapporto m/z. I diversi ioni vengono quindi raccolti da un collettore
(collector) alimentato con un voltaggio negativo e vengono rivelati da una lastra
fotografica nello spettrografo di massa, oppure da un elettromoltiplicatore o da un
fotomoltiplicatore nello spettrometro di massa. Lo strumento di Dempster il primo
spettrometro di massa che ha consentito di ottenere spettri in condizioni di discrete
sensibilit (per effetto della maggior resa ionica) e risoluzione (per effetto del campo di
accelerazione). Modulando da zero ad un valore prefissato - cio facendo la scansione
(scan) - sia di E che di H, si possono focalizzare tutte le specie ioniche sulla fenditura,
dopo averle generate nella sorgente e separate in base al rapporto m/z nellanalizzatore di
massa. A valle della fenditura c' un collettore che raccoglie, amplifica e registra le correnti
ioniche prodotte dai fasci di ioni positivi omologhi (cio con lo stesso m/z). Nello
spettrometro di Dempster veniva fatta la scansione del campo di accelerazione E, dal
momento che non era ancora possibile, tecnicamente, effettuare scansioni regolari e
riproducibili del campo magnetico H. In realt la scansione del voltaggio determina una
defocalizzazione dellion beam (detto detuning) per effetto delle diverse energie cinetiche
sovraimpresse a ioni di m/z differenti, mentre la scansione magnetica produce un effetto
contrario (tuning). La descrizione del funzionamento dellanalizzatore magnetico verr
trattata in un paragrafo successivo.
Spettrometria di massa
3. LA STRUMENTAZIONE MS
Impiegata inizialmente nello studio delle composizioni isotopiche, la spettrometria di massa
venne applicata alla chimica organica verso la met degli anni 30, per poi diffondersi
rapidamente negli anni 40 e 50. Ma quali erano le prestazioni degli spettrometri di massa
di quegli anni ? Lo spettrometro di massa prevedeva una sorgente ad impatto elettronico,
un analizzatore magnetico e un rivelatore spettroscopico. I campioni venivano introdotti
direttamente, se solidi, o tramite un serbatoio, se gassosi o liquidi. In queste condizioni si
potevano analizzare sostanze in un intervallo di massa (mass range) compreso tra 3 e
900 a.m.u. (atomic mass unit), con una risoluzione strumentale di 1.500-2.000. Sia allora che
oggi uno spettrometro di massa pu essere rappresentato con uno schema modulare (Fig. 9)
o con uno schema semiesploso (Fig. 10).
controllo strumentale
sistema di
introduzione
sorgente
ionica
analizzatore
di ioni
rivelatore e
registratore
sistema
del vuoto
Fig. 9 - Schema modulare di uno spettrometro di massa
sistema di
introduzione
sorgente
ionica
analizzatore
di ioni
rivelatore
di ioni
Fig. 10 Rappresentazione semiesplosa di uno spettrometro di massa
G. Bonaga
3.1. SISTEMA DEL VUOTO
Il sistema del vuoto - realizzato con pompe turbomolecolari, pompe a diffusione, pompe
criogeniche e pompe rotative, oggi di elevatissima efficienza, una componente
importantissima e delicata di tutto lapparato, dal momento che in molti casi la
spettrometria di massa (MS=Mass Spectrometry) non soltanto richiede un regime di alto
vuoto (10-5-10-8 Pa), ma un vuoto pulito, cio un vuoto nel quale siano trascurabili le
reazioni ione/molecola. Le reazioni ione/molecola, infatti, moltiplicano le combinazioni tra
le diverse specie chimiche (ioni e molecole) e lo spettro di massa che si otterrebbe sarebbe di
difficile interpretazione.
I diversi tipi di pompa da vuoto coprono differenti intervalli di pressione. Ogni tipo di
pompa caratterizzato dal valore della portata volumetrica (detta anche velocit di
pompaggio) e dal valore della minima pressione raggiunta (detta anche pressione limite). La
velocit di pompaggio dipende dalla pressione di ingresso della pompa e presenta sempre
un andamento decrescente al diminuire della pressione di lavoro. La pressione limite
misurata nel punto di ingresso della pompa e dal momento che tende a diminuire nel
tempo - perch si riduce nel tempo il flusso dei gas provenienti dal recipiente a vuoto - il
suo valore quello misurato quando la riduzione di pressione nel tempo risulta
trascurabile.
3.1.1. POMPA TURBOMOLECOLARE
Nella pompa turbomolecolare (Fig. 11), una serie di rotori cilindrici sui quali sono poste delle
lame (palette), ruotano ad alta velocit entro statori circolari, anchessi a lame. Le lame dei
rotori e degli statori sono opportunamente distanziate e inclinate in direzione opposta.
lame dello statore
motore
scarico
lame del rotore
rrotore
sospensione
magnetica
lubrificazione
Fig. 11 Pompa turbomolecolare
Per mezzo di un motore incorporato i rotori girano a velocit molto elevata (da 30.000 a
90.000 giri/min). L'azione pompante basata sul trasferimento della quantit di moto
dalla superficie delle lame in movimento alle molecole del gas da evacuare, per effetto
degli urti delle molecole gassose contro le lame, urti che incrementano notevolmente la
velocit delle molecole nella direzione di moto dello statore. A causa della differenza di
velocit tra le molecole provenienti dalla regione ad alto vuoto rispetto quelle provenienti
dalla regione a basso vuoto, la probabilit di trasmissione di molecole dalla regione ad alto
vuoto a quella a basso vuoto molto maggiore rispetto la trasmissione nella direzione
opposta, con la creazione di un regime di flusso di molecole che genera l'azione pompante.
La velocit della superficie in movimento deve essere sufficientemente alta per realizzare
10
Spettrometria di massa
la velocit ottimale di pompaggio, mentre la sequenza dei rotori e degli statori determina
il rapporto di compressione. Il profilo e le aperture delle lame sono disegnati in modo tale che
i ripetuti impulsi dati alle molecole le conducano sempre verso l'uscita della pompa, posta
di solito in basso e collegata ad una pompa diffusiva che provvede alla loro espulsione
all'esterno. Poich l'efficienza della velocit di trasferimento (energia cinetica) funzione
della massa delle molecole, la pompa turbomolecolare una pompa di frazionamento, ossia
pi efficace verso le molecole pi pesanti rispetto quelle pi leggere.
La velocit di pompaggio , quindi, in relazione al peso molecolare del gas, ma molto
elevata, fino a 4.000 l/s (pari a circa 15.000 m3/h).
La pressione limite di 10-10 Pa, ma la pompa turbomolecolare richiede sempre
laccoppiamento con una pompa da pre-vuoto che garantisca una pressione primaria di
10-1 Pa.
3.1.2. POMPA A DIFFUSIONE
La pompa a diffusione (Fig. 12), una pompa a pi stadi, con lo scarico tenuto a regime di
vuoto da una pompa meccanica primaria (10-1 Pa) collegata al recipiente da vuotare. Nella
pompa a diffusione un fluido riscaldato nel bollitore genera una corrente di vapori che
esce a velocit supersonica dai diffusori, opportunamente guidata verso una parete
raffreddata. Nel getto del primo stadio diffondono le molecole gassose provenienti dalla
pompa primaria e ricevono, per urto con le molecole del vapore, la quantit di moto
necessaria per giungere in prossimit del secondo stadio del diffusore dove ricevono una
seconda accelerazione dalle molecole del vapore, mentre il vapore condensa sulla parete e
ricade nel bollitore. In questo modo le molecole del gas da evacuare giungono allo scarico,
dove vengono aspirate da una pompa di prevuoto. Il principio di funzionamento
dunque basato sulla diffusione dei gas. La condensazione del vapore contrasta la
diffusione di quello operante, concorre alla corretta formazione dei getti e, infine, consente
il recupero del vapore che in questo modo viene sottoposto a una continua distillazione.
aspirazione
(dalla pompa primaria)
raffreddamento
ad acqua
diffusore
scarico
(alla pompa del prevuoto)
termostat
o
riscaldatore
dellolio
Fig. 12 Pompa a diffusione
11
G. Bonaga
La velocit di pompaggio dellordine di 3.000 l/s (pari a circa 10.000 m3/h).
La pressione limite coincide teoricamente con la tensione di vapore saturo del fluido
operante alla temperatura della parete raffreddata. Il primo fluido impiegato stato
il mercurio, ma oggi i fluidi pi usati sono:
- polialchilfenileteri (Neovac Sy): 10-8 Pa senza trappola;
- oli di silicone (Dow Corning 702 e 704, 705): rispettivamente da 10-6 , 10-8 e 10-10 Pa;
- polifeniletere a 5 anelli (Santovac): 10-10 Pa, per ultravuoto senza trappole perch di
bassissima volatilit e con il minimo rischio di retrodiffusione.
3.1.3. POMPA CRIOGENICA
La pompa crogenica (Fig. 13) si basa sul principio che una parete fredda esplica unazione di
pompaggio nei confronti di vapori e gas che, avendo un punto di ebollizione elevato,
hanno una tensione di vapore bassa alla temperatura della parete fredda.
Nella pompa criogenica, la pressione limite di un gas sempre superiore alla tensione di
vapore satura del gas alla temperatura della parete fredda.
Fig. 13 Pompa criogenica
Quando si impiega He liquido, la velocit di pompaggio diminuisce perch, per ridurre il
consumo di elio, il recipiente che lo contiene viene raffreddato con N2 liquido (a -196C),
allo scopo di ridurre lirraggiamento termico incidente sulla parete fredda.
La velocit di pompaggio pu arrivare a 2.000 l/s (pari a circa 7.000 m3/h), ma tende
a zero quando la pressione della camera a vuoto si avvicina alla pressione limite.
La pressione limite di 10-10 Pa, ma la pompa criogenica richiede laccoppiamento con
una pompa di pre-vuoto che garantisca una pressione di circa 10-1 Pa.
3.1.4. POMPA ROTATIVA
Le pompe rotative producono il vuoto primario (pre-vuoto) dellordine di 10-1 Pa e, nella
spettrometria di massa, sono sempre accoppiate con pompe a pi elevata efficienza
(turbomolecolari, a diffusione, criogeniche).
Nella pompa rotativa a pisone rotante (Fig. 14) lalbero del rotore coassiale con il tamburo
cilindrico, mentre il corpo del rotore (camma) eccentrico rispetto lalbero. Un pistone
12
Spettrometria di massa
cavo, comandato dalla camma, mette in comunicazione la camera a vuoto con il tamburo
cilindrico; la camma, nella rotazione, fa scorrere il pistone nella guida e mette
alternativamente la camera a vuoto in collegamento con la camera di compressione (fase
di aspirazione) e successivamente la isola (fase di compressione). Il rotore, durante il moto,
comprime i gas fino ad evacuarli nellatmosfera attraverso la valvola di scarico.
La velocit di pompaggio molto variabile, ma pu arrivare a 150 l/s (pari a circa
600 m3/h).
La pressione limite di 10-1 Pa.
Fig. 14 Pompa rotativa
3.1.5. CONFRONTO TRA LE PRESTAZIONI DELLE POMPE DA VUOTO
Nella tabella successiva vengono confrontate le caratteristiche delle pompe pi utilizzate
per ottenere il vuoto negli spettrometri di massa.
13
G. Bonaga
3.2. SISTEMI DI INTRODUZIONE DEI CAMPIONI
Allo scopo di analizzare un campione che a pressione artmosferica (760 torr), occorre
introdurlo nello spettrometro di massa in modo che il vuoto interno dello strumento
rimanga praticamente immodificato (10-7 torr). Tralasciando levoluzione storica dei sistemi
di introduzione, si pu proporre la classificazione pi attuale:
a. INTRODUZONE DIRETTA (EI, CI, ESI, APCI)
Sono sistemi di introduzione con i quali le tecniche di separazione (GC e HPLC) vengono
accoppiate con le sorgenti ioniche.
Lintroduzione da sistemi GC comunemente accoppiata alle sorgenti EI e CI (tramite
separator nel caso di colonne impaccate e tramite tranfert line nel caso di colonne
capillari). Lintroduzione da sistemi HPLC comunemente accoppiata a sorgenti ESI e
APCI.
b. INSERZIONE DIRETTA (MALDI, FAB)
Mediante un una sonda (probe) o un piastra (sample target) il campione viene inserito
direttamente nello strumento in un regime di vuoto mantenuto ai valori richiesti da valvole
di sicurezza. Successivamnte il campione viene sottoposto a processi di desorbimento,
tramite laser o per riscaldamento diretto, allo scopo di favorire la vaporizzazione e la
ionizzazione (di tipo diverso nel MALDI e nel FAB) delle molecole del campione.
3.2.1. ACCOPPIAMENTI GC/MS
3.2.1.1. COLONNE IMPACCATE
Nellaccoppiamento GC (colonne impaccate)-MS, leffluente dalla colonna passa attraverso
un separatore molecolare che ha la funzione di selezionare le molecole dellanalita dalle
molecole di solvente e di gas di trasporto, in modo che quelle dellanalit entrino con
traiettoria rettilinea nella sorgente ionica e quelle del solvente e del gas di trasporto
vengano evacuate dal sistema del vuoto. Lo splittaggio del solvente contribuisce a rendere
compatibile la pressione della sistema GC (praticamente a pressione atmosferica) con il
sistema di alto vuoto della MS (10-7 torr). I pi comuni sono quello di vetro poroso di
Watson-Biemann (Fig. 15), a jet di Ryhage-Stenhagen (Fig. 16), ma anche a membrana (Fig.
17) e di Brunnee (Fig. 18).
Fig. 15 - Separatore di Watson Biemann
Fig. 16 - Separatore di Ryhage Stenhagen
14
G. Bonaga
Fig. 17 - Separatore a membrana
Fig. 18 - Separatore di Brunnee
3.2.1.2. COLONNE CAPILLARI
Nell'accoppiamento GC (colonne capillari)-MS (Fig. 19), un tubo capillare in silice fusa
(privo di liquido di partizione) funziona da linea di trasferimento (transfert line)
delleffluente; il tubo entra nello spettrometro e viene normalmente posizionato in modo
che le molecole emergano con geometria perpendicolare alla direzione dellelectron beam.
La compatibilit tra il settore GC a pressione e il settore MS in regime di vuoto (10-7 torr),
viene garantita da pompe da vuoto ad alta efficienza (turbomolecolari).
MS
sorgente ionica
transfert
line
line
GC
vuoto
(pompa turbomolecolare)
Fig. 19 - Accoppiamento HRGC/MS
3.2.2. ACCOPPIAMENTI LC/MS
Sono sistemi di introduzione associati a specifiche sorgenti ioniche (ESI, APCI), diffusi
nellaccoppiamento HPLC-MS. Verranno discusse nella sezione che illustra le diverse
sorgenti ioniche.
14
Spettrometria di massa
3.2.3. INTRODUZIONE DIRETTA IN SORGENTE (MALDI, FAB)
La maggior parte dei materiali biologici sono altobollenti, ma bisogna considerare che, in
base alle costanti cinetiche di decomposizione e di vaporizzazione, alle alte temperature
favorito il processo di vaporizzazione se il trasferimento di energia termica rapido (Fig.
20).
ln v
decomposizione
vaporizzazione
1/T
Fig. 20 - Velocit di decomposizione e di vaporizzazione
I solidi vengono introdotti (Fig 21) tramite una sonda (probe) nella cui estremit cava
pu alloggiare un capillare contenente la sostanza solida.
Fig. 21 - Direct Inlet
Un premistoppa di teflon garantisce la tenuta, mentre un sistema di riscaldamento
dedicato esclusivamente alla sonda pu produrre un incremento di temperatura fino a circa
300C; al valore di vuoto abituale del sistema (~ 10-7 torr) questa temperatura determina la
distillazione (volatilizzazione) della maggior parte delle sostanze organiche solide, senza
decomposizione.
15
G. Bonaga
Indipendentemente dal sistema di introduzione del campione, sovente associato ad una
particolare sorgente ionica, le teorie e i principi della spettrometria di massa devono
rispondere ai numerosi quesiti che accompagnano il cammino delle molecole del campione,
a partire dalla sorgente ionica fino ad arrivare al rivelatore degli ioni.
SISTEMI DI IONIZZAZIONE (sorgenti ioniche)
- dove si ionizzano le molecole ?
- in che modo ?
- dove si frammentano ?
- in che modo ?
- quali fattori governano la framentazione ?
SISTEMI DI SEPARAZIONE (analizzatori)
- dove si separano gli ioni prodotti in sorgente ?
- in che modo ?
SISTEMI DI RIVELAZIONE (rivelatori e registratori)
- dove vengono rilevati gli ioni ?
- in che modo ?
- come vengono registrati i segnali prodotti ?
16
Spettrometria di massa
3.3. IONIZZAZIONE E SORGENTI IONICHE
La ionizzazione il processo, che avviene nella sorgente ionica, per effetto del quale le
molecole neutre si trasformano in particelle cariche. Si possono ionizzare le molecole neutre
(per espulsione di elettroni, cattura di elettroni, protonazione, cationizzazione,
deprotonazione) o trasferire le molecole cariche da una fase condensata a una fase gassosa.
METODO DI IONIZZAZINE
emissione di elettroni
(ioni positivi)
cattura di elettroni
(ioni negativi)
protonazione
(ioni positivi)
deprotonazione
(ioni negativi)
cationizzazione (Na+ o K+)
(ioni positivi)
trasferimento di molecole cariche in
fase gassosa
(ioni positivi e negativi)
EMISSIONE DI ELETTRONI
CATTURA DI ELETTRONI
PROTONAZIONE
17
ACRONIMO
EI
EI
CI, ESI, APCI,
MALDI, FAB
ESI, APCI,
MALDI, FAB
ESI, APCI,
MALDI, FAB
ESI, APCI,
MALDI, FAB
VANTAGGI E SVANTAGGI
fornisce lo ione molecolare e gli ioni frammenti
eccesso di frammentazione
fornisce lo ione molecolare e gli ioni frammenti
eccesso di frammentazione
molte sostanze non si protonano (idrocarburi) o
sono instabili nella forma protonata (glucidi)
limitata a sostanze a carattere acido
carenza o assenza di frammentazione
limitata a ioni gi prodotti
G. Bonaga
DEPROTONAZIONE
CATIONIZZAZIONE
TRASFERIMENTO DI MOLECOLE CARICHE IN FASE GASSOSA
La ionizzazione delle molecole neutre nella sorgente ionica si pu ottenere mediante
particelle primarie, quali elettroni (EI), cationi (CI, APCI), atomi (FAB), fotoni (MALDI),
oppure con campi elettrici (FI, FD).
18
Spettrometria di massa
La trasformazione delle molecole organiche neutre in ioni positivi o negativi il tipo di
spettrometria di massa pi diffuso; i processi che producono gli ioni positivi e negativi
possono essere cos riassunti:
POSITIVE-IONS
M + e- M +.
M + e- M ++
M + e- M +++.
+ 2e- (molto probabile)
+ 3e- (poco probabile)
+ 4e- (molto improbabile)
NEGATIVE-IONS
M + e- M M + e- (M-Y) - + Y .
M + e- (M-Y) - + Y +.+ e -
(0-2 eV)
(2-10 eV)
(> 10 eV)
La resa in ioni positivi sensibilmente superiore a quella in ioni negativi:
M /M 1.000
anche se entrambi gli spettri di massa sono di grande utilit nello studio della struttura dei
composti organici. La ionizzazione delle molecole neutre nella sorgente ionica, sebbene
possa essere effettuata in modi molto diversi, ha comunque due obiettivi principali
1. produrre una resa elevata di ioni positivi o negativi;
2. collimare il fascio di ioni positivi o negativi che si forma in sorgente.
Le sorgenti ioniche, indipendentemente dal tipo, devono :
1. avere unelevata efficienza, cio devono fornire unelevata resa ionica (+ o -) ed un
elevato coefficiente di trasmissione degli ioni prodotti;
2. originare fasci ionici monoenergetici e di intensit costante;
3. produrre un elevato rapporto segnale/rumore (signal/noise);
4. avere scarsa memoria, cio non devono rimanere contaminate dalle molecole dei
campioni precedentemente analizzati.
sorgente EI
sorgente APCI
19
sorgente ESI
sorgente MALDI
G. Bonaga
3.3.1. SORGENTE A IMPATTO ELETTRONICO (Electron Impact = EI)
La rappresentazione schematica della ionizzazione per impatto elettronico mostrata in
Fig. 22.
Fig. 22 - Collisione elettrone/molecola nella EI
La sorgente EI (Fig. 23) la pi impiegata nello studio dei composti organici anche se,
essendo una ionizzazione hard, non idonea a tutti i composti e comporta una intensa
frammentazione dello ione molecolare.
Fig. 23 - Sorgente EI
Il fascio di elettroni (electron beam) viene prodotto da un filamento di renio (o tungteno)
riscaldato a circa 300C, in un regime di vuoto di circa 10-7 torr che ha lo scopo di evitare le
collisioni ione-molecola, collisione capaci di produrre una quantit di ioni di origine
secondaria talmente elevata che renderebbe difficilmente interpretabile lo spettro di massa.
Gli elettroni emessi dal filamento vengono accelerati dalle pareti della camera di
ionizzazione, mediante un potenziale positivo compreso tra 50 e 75 V, e vengono raccolti da
un collettore che ha una d.d.p. con le pareti della camera di ionizzazione di circa 10-30 V.
Lallineamento del fascio elettronico mantenuto da un campo magnetico esterno di circa
10 gauss che determina una traiettoria a spirale degli elettroni emessi dal filamento. Le
molecole del campione entrano nella camera di ionizzazione e gli elettroni che possiedono
unenergia superiore allenergia di ionizzazione delle molecole determinano la formazione
degli ioni positivi. Gli elettroni hanno una probabilit definita di ionizzare le molecole
neutre del campione gassoso, probabilit che dipende dallintensit del fascio elettronico e
dalla densit del campione gassoso e che determina lintensit della corrente di ioni positivi
che si origina (dellordine di 10-10A). Il fascio di ioni positivi (ion beam) raggiunge la
fenditura di uscita della sorgente ionica e gli ioni vengono accelerati dagli estrattori che
hanno voltaggio positivo (tra essi e la camera di ionizzazione mantenuta una d.d.p. di
20
Spettrometria di massa
alcuni kV); lion beam viene focalizzato dalle lenti di focalizzazione e collimato dalle lenti di
collimazione, in modo che il fascio di ioni positivi abbia la massima trasmissione attraverso
la fenditura . Le specifiche pi importanti della sorgente EI possono essere cos riassunte:
ionizzazione energica per impatto; 10-7 torr, temperatura elevata;
intensit variabile dello ione molecolare (da 0 a 100%);
intensit elevata degli ioni-frammento;
sensibilit elevata (ng, pg);
particolarmente indicata per: composti organici gassosi o gassificabili, termostabili, apolari o
resi tali.
3.3.2. SORGENTE A IONIZZAZIONE CHIMICA (Chemical Ionization = CI)
La rappresentazione delle collisioni che intervengono nella CI mostrata nella Fig. 24.
Fig. 24 - Collisioni elettrone/gas, ione gas/gas e ione gas/molecola
Il chimismo della ionizzazione chimica, se si impiega il metano come gas reagente, il seguente:
1. CH4 + e- =
+
2a. CH4 + CH4 =
2b. CH3+ + CH4 =
2c. [CH2+ + CH4 =
C2H3+ + CH4 =
CH4+ + 2e+
CH3 + CH5
H2 + C2H5+
H2 + C2H3+]
H2 + C3H5+
~ 46%
~ 41%
~ 5%
Gli ioni CH5+ (donatori di 1 a.m.u.), C2H5+ (29 a.m.u.) e C3H5+ (41 a.m.u.) non sono reattivi
nei confronti del CH4, ma reagiscono con le molecole del campione per formare i
corrispondenti ioni quasi-molecolari nel rapporto quantitativo corrispondente:
(M+1)+ ; (M+29)+ ; (M+41)+
Nella sorgente CI (Fig. 25) le molecole gassose del campione vengono ionizzate per
collisione con gli ioni di un plasma, ottenuto per impatto elettronico di un gas di reazione
immesso nella sorgente alla pressione di circa 1 torr. Il gas di reazione (metano,
ammoniaca, isobutano, ecc.) deve produrre ioni che, oltre a reagire blandamente con le
molecole neutre dello stesso tipo di quelle da cui derivano, siano in grado di reagire con le
molecole neutre del campione, introdotto nella sorgente ionica alla pressione di 10 -4 torr,
per dare degli ioni quasi-molecolari.
21
G. Bonaga
Fig. 25 - Sorgente CI
La sorgente CI differisce da quella EI per la minor dimensione sia della fenditura di
ingresso degli elettroni che della fenditura di uscita dellion beam; inoltre il regime del
vuoto deve inizialmente favorire le reazioni ione-molecola (contrariamente alla sorgente
EI), ma successivamente deve garantire unelevata velocit di pompaggio dei volumi da
evacuare, in modo da realizzare la caduta di pressione dal valore in sorgente (circa 1 torr)
al valore dellanalizzatore di massa (10-6-10-7 torr). Le specifiche pi importanti della
sorgente CI possono essere cos riassunte:
-4
ionizzazione blanda ione-molecola; 10 torr; temperatura elevata;
intensit elevata dello ione quasi-molecolare;
intensit bassa degli ioni-frammento;
sensibilit elevata (ng, pg);
particolarmente adatta per: composti organici gassosi o gassificabili, termostabili, apolari .
3.3.3. SORGENTE A IONIZZAZIONE DI CAMPO (Field Ionization = FI)
Nella sorgente FI (Fig. 26) le molecole gassose del campione vengono ionizzate per effetto
di un campo elettrico di circa 10-7-10-8 V.cm-1. La sorgente costituita da un anodo
puntiforme detto emitter, generalmente di platino, e da un catodo cilindrico in cui si apre
una fenditura. La probabilit della ionizzazione cresce con la forza del campo e pertanto
esiste un valore-soglia al di sotto del quale la corrente prodotta dagli ioni positivi non
misurabile.
E
Fig. 26 - Sorgente FI
In un campo elettrico elevato la curva potenziale della molecola neutra del campione viene
distorta da un effetto tunnel che produce la perdita di un elettrone; questo elettrone viene
catturato da un orbitale vuoto dellemitter metallico, generalmente costituito da fili di
platino attivati. Lattivazione consiste nel ricoprirlo con microcristalli a forma di aghi
prodotti da un solvente (acetone, benzonitrile, ecc.) che viene immesso in sorgente prima
22
Spettrometria di massa
dellanalisi del campione. La pressione in sorgente dellordine di 3 . 10-3 torr ed i voltaggi
si aggirano attorno ai 10 kV. Gli ioni positivi che si formano per trasferimento di un protone
vengono accelerati dagli estrattori E con energie di alcuni keV. Lion beam risulta per
talmente disperso che le operazioni relative alla sua focalizzazione e collimazione (con le
lenti FL e CL) nella fenditura S non sono facili, tanto che la sensibilit delle sorgenti
FI risulta decisamente inferiore a quella della sorgente EI. Le specifiche pi importanti della
sorgente FI possono essere cos riassunte:
ionizzazione blanda per tensione elettrica (10-1 eV); 10-3 torr;
intensit elevata dello ione quasi-molecolare;
intensit bassa degli ioni-frammento;
sensibilit scarsa (mg, g);
particolarmente adatta per: composti organici gassosi e gassificabili che danno solo [M+1]+
(idrocarburi e prodotti di pirolisi).
3.3.4. SORGENTE A DESORBIMENTO DI CAMPO (Field Desorption = FD)
Nella sorgente FD (Fig. 27) i composti solidi depositati sullemitter vengono ionizzati per
azione di forti campi elettrici (alcuni kV) e desorbiti come ioni positivi per trasferimento di
un protone sulla molecola di analita. In genere lemitter costituito da nichel supportato
da tungsteno, od anche da solo tungsteno, ricoperto da microaghi carboniosi.
E
Fig. 27- Sorgente FD
Lemitter mobile e viene immerso in una soluzione (o sospensione) di analita, ovvero una
goccia di campione viene depositata sullemitter, dopodich lemitter viene ricollocato nella
sorgente ionica. Il fascio ionico viene focalizzato immettendo vapori di acetone o di altro
solvente volatile nella sorgente che viene usata come la FI e successivamente, dopo
eliminazione del solvente, si stabilisce una d.d.p. tra anodo e catodo - distanti solo alcuni
millimetri - di circa 10 kV. La caratteristica principale della sorgente FD che essa non
richiede la preventiva gassificazione del campione; in presenza di campi elettrici forti,
infatti, lenergia di desorbimento di campo degli ioni molto piccola rispetto allenergia di
sublimazione. Le specifiche pi importanti della sorgente FD possono essere cos riassunte:
ionizzazione blanda per tensione elettrica (10-1 eV) e desorbimento degli ioni prodotti;
10-3 torr; temperatura bassa;
intensit elevata dello ione quasi-molecolare;
sensibilit scarsa (g, mg);
particolarmente adatta per: composti organici solidi o poco volatili, termolabili (polipeptidi a 9
unit, sali organici).
23
G. Bonaga
Esempio 1: prolina (mol wt = 115)
Gli spettri di massa della prolina (Fig. 28) registrati con sorgente EI e CI, mostrano che nel
primo caso lo ione molecolare non sufficientemente stabile per dare origine ad un segnale,
mentre nel secondo caso lo ione quasi-molecolare il picco-base dello spettro. I due diversi
schemi di frammentazione sono riportati nella Fig. 29.
EI
CI
Fig. 28 - Spettri di massa della prolina: EI e CI
Fig. 29 - Schema di frammentazione della prolina con sorgenti EI e CI
24
Spettrometria di massa
Esempio 2: creatina (mol wt 131)
Gli spettri di massa della creatina (Fig. 30 e Fig. 31) registrati impiegando sorgenti EI, CI, FI
e FD, dimostrano che nei primi tre casi non possibile ottenere il segnale corrispondente
allo ione molecolare (m/z 131), mentre nel caso della sorgente FD lo ione quasi-molecolare
(m/z 132) il picco-base dello spettro. I quattro diversi schemi di frammentazione del
composto sono riportati nelle Fig. 32 e Fig. 33.
Fig. 30 - Spettri di massa della creatina: EI e CI
114
Fig. 31 - Spettri di massa della creatina: FI e FD.
Modelli Balls and Sticks e Spacefill della creatina
25
G. Bonaga
Fig. 32 - Schema di frammentazione della creatina con sorgenti EI e CI
26
Spettrometria di massa
Fig. 33 - Schema di frammentazione della creatina con sorgenti FI e FD
27
G. Bonaga
3.3.5. ELECTROSPRAY ( Electrospray Ionization = ESI)
oggi il metodo di ionizzazione che, insieme all Atmospheric Pressure Chemical Ionization
(APCI), consente l'ottimale accoppiamento della spettrometria di massa con la LC, perch
la ionizzazione viene fatta a pressione atmosferica e a bassa temperatura. LESI si basa sul
principio che un voltaggio di un ago produce in un fluido un gradiente elettrico che
determina la migrazione delle cariche in superficie. Il liquido emerge dallago, la cui punta
agisce da filamento e quando la tensione superficiale del liquido eguaglia la repulsione
elettrostatica, le goccioline contenenti gli ioni positivi (o negativi), bombardate da un gas
inerte, si staccano dal filamento e formano un "jet" che produce uno "spray" di goccioline
nebulizzate contenenti gli ioni.
La sorgente ESI (Fig. 34) costituita essenzialmente da due elettrodi; il capillare d'acciaio
ESI ed il piatto ("curtain plate"), tra i quali una differenza di potenziale di circa 3,0 kV
(variabile da 1,5-5,0 kV) e un flusso di N2 ("nebulizer gas") producono lo spray (Fig. 35) di
goccioline (~ 1 m) contenenti gli ioni. Per desolvatazione le goccioline si contraggono e
rimpiccioliscono (~ 10 nm) fino a quando le repulsioni elettrostatiche tra gli ioni (dello stesso
segno) prevalgono sulla tensione superficiale delle goccioline: avviene allora un'esplosione
columbiana, con formazione di ioni quasi molecolari [M+nH]n+. Gli ioni, focalizzati da un
elettrodo (skimmer), vengono accelerati in direzione dellanalizzatore Q0.
Fig. 34 Sorgente ESI
Molti solventi possono essere impiegati nellESI, ma la scelta di quello pi idoneo deve
essere fatta in funzione della solubilit degli analiti, della volatilit del solvente e della sua
abilit a donare protoni. I solventi pi comuni sono metanolo/acqua (50/50) e
acetonitrile/acqua (50/50).
28
Spettrometria di massa
evaporazione
del solvente
fissione
esplosione
coulombiana
formazione di ioni per ulteriore
fissione e/o evaporazione
Fig. 35 Formazione dello spray e degli ioni multicarica
Contrariamente agli altri accoppiamenti LC-MS, lESI risulta una ionizzazione ad elevata
sensibilit, con una risposta direttamente proporzionale allanalita che entra nella
sorgente, indipendentemente dalla velocit di flusso a cui viene erogato. LESI pu essere
impiegata anche per molecole di piccole dimensioni e per composti a bassa polarit,
sebbene le applicazioni pi diffuse riguardano molecole ad alto peso molecolare,
termolabili, polari (peptidi, proteine, oligonucleotidi, ecc.). La sua caratteristica di essere
una ionizzazione soft ne consente limpiego nello studio di composti a struttura labile,
dal momento che questi si possono ionizzare senza alterare la loro struttura. Non
intervenendo alcuna frammentazione degli ioni, gli spettri di massa ottenuti con la
ionizzazione ESI non forniscono informazioni strutturali, ma in prima istanza forniscono
informazioni sul peso molecolare dellanalita. Per questo motivo frequente che a questa
tecnica venga convenientemente associata una spettrometria di massa tandem (MS/MS).
Le principali caratteristiche dellESI sono:
spettri con informazioni sul mol wt
elevata sensibilit
idonea per analiti volatili e non volatili ionici e/o polari non volatili
nessuna frammentazione indesiderata
idonea alla determinazione di alti pesi molecolari
particolarmente idonea alla HPLC
La Fig. 36 riporta lo spettro ESI del resveratrolo (mol wt 228) a basso voltaggio (25 V) in
modalit negativa.
29
G. Bonaga
[M] -
Fig. 36 Spettro ESI del resveratrolo in modalit negativa
3.3.6. NANOELECTROSPRAY ( Nanoelectrospray Ionization = NanoESI)
La sorgente ionica simile allESI, ma lago dello spray molto piccolo ed posizionato
allentrata dellanalizzatore di massa; il risultato di questi accorgimenti (basso flusso di
effluente e incremento della trasmissione di ioni nello spettrometro) un notevole
incremento di efficienza , che comporta la riduzione della quantit di campione necessaria
per lanalisi. I flussi del NanoESI sono dellordine di 10-100 nl/minuto, valori che si
ottengono impiegando degli emitters, di vetro soffiato o metallizzato od anche di silice
fusa, il cui orifizio talmente piccolo (~ 5m) da produrre uno spray di goccioline molto
piccole (~ 0,2 m). La dimensione ridotta delle goccioline richiede una minore evaporazione
per la formazione degli ioni, ma la minore evaporazione evita anche la concentrazione dei
sali e delle altre impurezze, rendendo il NanoESI pi tollerante rispetto il grado di purezza
del campione. La Fig. 36bis riporta lo spettro di massa con sorgente NanoESI di un
policloroalchilsolfato.
Fig. 36bis Spettro NanoESI in modalit negativa di un policloroalchilsolfato
30
Spettrometria di massa
3.3.7. IONIZZAZIONE CHIMICA A PRESSIONE ATMOSFERICA (Atmospheric Pressure
Chemical Ionization = APCI)
Il successo della sorgente APCI (Fig. 37) dovuto al fatto che essa particolarmente adatta
ad analizzare i composti organici non volatili, molto diffusi nel settore farnaceutico,
biomedico e ambientalistico. Inoltre questa sorgente si adatta benissimo allaccoppiamento
LC/MS dal momento che alla considerevole efficienza a valori di flusso elevati (2 ml/min)
unisce anche unottima sensibilit e linearit della risposta.
Con lAPCI si generano ioni direttamente dalla soluzione, ma contrariamente allESI
leffluente viene introdotto direttamente nella sorgente ionica. Le goccioline dei soluti non
sono cariche e la sorgente, dotata di un source heater, favorisce la loro
desolventazione/vaporizzazione. Le molecole vaporizzate sono trasportate nella regione a
pressione atmosferica nella quale un elettrodo a corona daghi provvede alla
ionizzazione delle molecole del solvente che a loro volta producono la ionizzazione del
gas chimico. Poich gli ioni del gas chimico sono a pressione atmosferica le collisioni tra gli
ioni del gas chimico e le molecole dei soluti sono molto probabili e frequenti, quindi la
ionizzazione dei soluti molto efficiente. Nella modalit positiva la molecola del soluto
acquista un protone dal gas chimico e forma uno ione quasi molecolare [MH]+; nella
modalit negativa la molecola del soluto cede un protone al gas chimico e forma lo ione
quasi-molecolare [M-H]-.
La modesta influenza del solvente sugli ioni del gas chimico e lelevata pressione riducono
la frammentazione degli ioni molecolari dei soluti, con il grande vantaggio di poter
dedurre, dallo spettro di massa, il loro peso molecolare. Il principio base dunque quello
della ionizzazione chimica dellanalita, ma contrariamente alla classica sorgente CI la
reazione viene condotta a pressione atmosferica.
LAPCI costituita da tre sezioni:
1. regione della sonda di nebulizzazione (a pressione atomosferica);
2. regione della ionizzazione a corona daghi (a presione atmosferica);
3. regione dellaccelerazione e della focalizzazione degli ioni (a pressione intermedia).
La terza regione interfacciata direttamente con un analizzatore quadrupolare che opera in
regime di alto vuoto.
Fig. 37 - Sorgente APCI
31
G. Bonaga
Il flusso totale (solvente ed analita) di fase mobile proveniente dalla LC entra, tramite un
capillare, nella sonda (probe), nella quale viene nebulizzata da un flusso di N2 (nebulizer
gas). Laerosol viene fatto progredire fino allestremit riscaldata della sonda da un altro
flusso di N2 (sheath gas); il riscaldamento trasforma la fase mobile liquida in fase gassosa
che viene trasferita nella regione di ionizzazione da un ulteriore flusso di N 2 (bath gas).
Qui una temperatura di circa 120C evita la condensazione del vapore, mentre una d.d.p. di
circa 2 kV tra lelettrodo di scarica a corona d'aghi (corona discharge electrode) e lelettrodo
contatore (counter electrode) determina un cono di ionizzazione che produce prima la
ionizzazione di N2, quindi la formazione dei radicali-ioni del solvente ed infine il
trasferimento di protoni dal reagente chimico alle molecole neutre dellanalita o viceversa.
Gli ioni passano, attraverso la chicane dellelettrodo contatore, nella regione a pressione
intermedia ( = 1 mbar), nella quale il solvente e il gas di trasporto evaquano, mentre gli ioni
dellanalita vengono accelerati da un potenziale di 10-100 V ottenuto da una placca
(skimmer) e, focalizzati dallottica di trasferimento (transfert optics), entrano
nellanalizzatore quadrupolare. I processi che producono gli ioni dellanalita nella sorgente
APCI , con il benzene come solvente, sono:
N2 + eN2+. + N2
N4+. + C6H6
C6H6+. + M
= N2+. + 2e= N4+
= 2N2+ C6H6+.
= C6H5. + [M + H]+
La Fig. 38 riporta lo spettro di massa APCI della sulfametazina e la Fig. 39 la relativa
frammentazione.
Fig. 38 - Spettro di massa APCI della sulfametazina registrato a Vc = 80V
32
Spettrometria di massa
Fig. 39 Schema di frammentazione della sulfametazina
33
G. Bonaga
3.3.8. DESORBIMENTO/IONIZZAZIONE LASER ASSISTITA DA MATRICE (MatrixAssisted Laser Desorption/Ionization = MALDI)
stato introdotto nel 1988, specialmente per ottimizzare lanalisi di sostanze naturali
termolabili, polari, non volatili e di peso molecolare elevato (proteine, peptidi, glucidi,
oligonucleotidi, lipidi, ecc.).
Nonostante il meccanismo esatto del desorbimento/ionizzazione del MALDI non sia ancora
noto, accreditata la tesi che la ionizzazione e il desorbimento dellanalita dalla fase
condensata alla fase gassosa avvenga per eccitazione laser della miscela campione/matrice.
Lanalita viene co-critallizzato con un eccesso molare di una matrice contenente dei
cromofori UV-assorbenti (acidi organici deboli) e la miscela matrice/analita viene irradiata
con i fotoni (UV = 337 nm) prodotti da un laser pulsato. Le radiazioni vengono trasformate
in energia di eccitazione delle molecole di matrice la quale, essendo solida, protegge anche
lanalita, eventualmente sensibile, dalle radiazioni incidenti. La matrice produce la
ionizzazione delle molecole di analita per protonazione o per cationizzazione, durante il
desorbimento. La frammentazione degli ioni dellanalita impedita o minimizzata perch la
matrice trasferisce agli ioni unenergia vibrazionale minima.
Fig. 40 Deposizione del campione nel MALDI
Le procedure di preparazione della miscela matrice/campione hanno grande influenza sul
risultato dellanalisi. Il metodo pi usato quello che prevede la miscelazione di una
soluzione satura di matrice alla soluzione di analita nel rapporto 5000/1. Unaliquota di
questa miscela viene applicata sulla piastra (sample target) e fatta cristallizzare in aria
secca. Le matrici pi diffuse, in funzione della natura del campione, sono:
peptidi:
acido -ciano-4-idrossicinnamico [1] in ACN/H2O (50/50)
con 0,1% di acido trifluoroacetico (TFA);
proteine, macromolecole:
acido sinapinico [2] in ACN/H2O con 0,1% di TFA;
glicoproteine, molecole piccole: acido 2,5-idrossibenzoico [3] in ACN/H2O (50/50).
34
Spettrometria di massa
Gli ioni dellanalita che passano in fase gassosa vengono accelerati per mezzo di un alto
voltaggio in direzione dellentrata dellanalizzatore di massa, un Time of Flaying (TOF)
che separa gli ioni in base al tempo di volo degli ioni aventi diversi valori di m/z. La natura
pulsata del MALDI compatibile soltanto con una analizzatore TOF perch linizio del
tempo di volo degli ioni pu essere fatto coincidere con ciascuna pulsazione laser e
terminare quando tutti gli ioni hanno raggiunto il detector. Negli altri analizzatori di massa
(magnetico, quadrupolare), invece, il flusso di ioni continuo e pertanto incompatibile con
la natura pulsata della ionizzazione MALDI.
Fig. 41 MALDI/TOF
Fig. 42 Spettro di massa MALDI di -lattoalbumina
35
G. Bonaga
3.3.9. IONIZZAZIONE PER BOMBARDAMENTO CON ATOMI VELOCI (Fast Atom
Bombardment = FAB)
Nel 1981 stato introdotto il FAB (Fig. 44), una sorgente simile al MALDI perch utilizza
una matrice liquida (anzich solida cristallina) e un fascio di particelle per il desorbimento
degli ioni dalla superficie, ma mentre il MALDI impiega un fascio di luce laser pulsato, il
FAB utilizza un fascio continuo. Il FAB ha una sensibilit 1000 volte inferiore al MALDI. La
ionizzazione con atomi o ioni veloci una ionizzazione soft che viene fatta introducendo
direttamente il campione nella sorgente ionica tramite una sonda. Un fascio
sufficientemente veloce di atomi di Xe (o Ar) o di ioni Cs+ producono la protonazione
[MH]+ o la cationizzazione [MNa]+ delle molecole neutre dellanalita. La matrice che
produce la ionizzazione e il desorbimento un materiale liquido non volatile che rifornisce
la superficie di nuovo campione da sottoporre al bombardamento con il fascio di atomi (o di
ioni) incidenti. Per assorbimento della maggior parte dellenergia incidente, la matrice
preserva o minimizza la degradazione degli ioni quasi-molecolari che si formano
dallanalita. Il campione in soluzione viene introdotto nella sorgente ionica ad una
pressione di 10-5-10-6 torr e sottoposto ad una corrente di 2-10 kV; in queste condizioni si
forma un plasma di molecole. Il plasma viene bombardato da un fascio di atomi (atom
beam, generalmente prodotto da Argon o Xenon gassosi) che vengono sparati da un
cannone (FAB gun). Una parte di atomi bombardanti (fast atoms) provvista
dellenergia sufficiente a ionizzare le molecole neutre, altri no (slow atoms). Gli ioni dotati
di maggiore energia (fast ions) attraversano, senza essere deviati, il campo elettrostatico
prodotto dai deflettori e vengono raccolti dal rivelatore, quelli a energia minore si
neutralizzano sul deflettore (deflector).
Fig. 44 - Sorgente FAB
Le due matrici pi comuni sono:
CH2OH
NO2
alcol m-nitrobenzilico
(NBA)
CH2OH
HO C H
CH2OH
glicerolo
36
Spettrometria di massa
Gli atomi veloci e gli ioni collidono con la matrice producendo il desorbimento nellanalita
nella fase gassosa. Lanalit pu caricarsi e trasferirsi nella fase gassosa o caricarsi durante il
desorbimento per reazione con le molecole o gli ioni circostanti. Nella fase gassosa gli ioni
vengono accelerati elettrostaticamente per essere immessi nellanalizzatore di massa.
I vantaggi del FAB sono dovuti al fatto che il campione in soluzione d origine a segnali
ionici persistenti; inoltre la resa ionica talmente elevata che anche le sostanze poco volatili
non richiedono alte temperature per fornire la quantit di ioni necessaria alla registrazione
di uno spettro di massa.
Con il FAB si possono ottenere:
1) radicali-ioni, (da composti non polari);
2) ioni protonati (da composti polari)
3) ioni preformati in soluzione (da composti organometallici)
Queste tre possibilit rendono questa tecnica di ionizzazione molto pertinente nellanalisi di
composti naturali organometallici, specialmente vitamine, coenzimi, pigmenti, polipeptidi,
ecc.
La Fig. 45 riporta lo spettro di massa FAB del composto organometallico C27H28P2Pt (con
194Pt il mol wt 608), mentre la Fig. 46 riporta lo spettro di massa FAB (parziale) della
vitamina B12, che ha peso molecolare 1354.
Fig. 45 - Spettro di massa (parziale) FAB del C27H28P2Pt
Fig. 46 - Spettro di massa FAB (parziale) della vitamina B12
37
G. Bonaga
3.3.9. CONFRONTO TRA LE CARATTERISTICHE DELLE SORGENTI IONICHE
Viene riportato (Fig. 47) il ripilogo della sensibilit e del mass range delle sorgenti ioniche
che sono state illustrate.
Fig. 47 Sensibilit e mass range delle tecniche di ionizzazione
38
Spettrometria di massa
3.4. SISTEMI DI SEPARAZIONE DEGLI IONI
Sono gli analizzatori (analyzer), che separano gli ioni in funzione della loro rapporto
massa/carica. Gli analizzatori si possono suddividere in 2 gruppi:
a) ANALIZZATORI STATICI (magnetico)
Separano gli ioni in base alla loro quantit di moto, cio con valori diversi del prodotto mv.
b) ANALIZZATORI DINAMICI (quadrupolare, tempo di volo)
Separano gli ioni in dipendenza del tempo stabilito per uno o pi parametri del sistema
analizzatore.
Le prestazioni di uno spettrometro di massa sono strettamente connesse al tipo di
analizzatore impiegato; queste prestazioni riguardano principalmente la sensibilit (cio la
quantit minima di composto dalla quale si pu ottenere uno spettro di massa
interpretabile) e il potere risolvente o risoluzione (cio la capacit di distinguere e di rivelare
ioni che differiscono anche di pochissimo nel rapporto m/z). La risoluzione la specifica
fondamentale per misurare la massa esatta delle diverse specie ioniche
a) ANALIZZATORI STATICI
Gli studi teorici di Mattauch, Herzog ed altri hanno dimostrato che la risoluzione di uno
spettrometro di massa con analizzatore statico funzione di 4 fattori:
1. DIVERGENZA DEL FASCIO IONICO
E dovuta alle traiettorie diverse degli ioni che si formano nella sorgente e che entrano nella
regione dellanalizzatore con direzioni comprese in un certo angolo , come mostra la Fig.
48 (mancanza di focalizzazione della direzione).
Fig. 48 - Divergenza dellelectron beam
2. DISTRIBUZIONE DELLE ENERGIE CINETICHE
E dovuta a ioni che hanno la stessa massa, ma energie cinetiche diverse, dal momento che il
potenziale (V) disomogeneo della sorgente sottopone gli ioni a campi di accelerazione
diversi, come mostra la Fig. 49 (mancanza di focalizzazione dellenergia);
mv2/2 = zV
39
G. Bonaga
Fig. 49 - Distribuzione delle energie cinetiche
3. RAGGIO DI CURVATURA DELLA TRAIETTORIA DEGLI IONI
Il raggio di curvatura della traiettoria degli ioni nel settore magnetico determinato dal
profilo e dalla sezione del magnete impiegato (deflessione magnetica).
Assumendo che:
tutti gli ioni con uguale massa ed energia che attraversano il campo magnetico
convergono nello stesso fuoco:
i campi di contorno siano trascurabili;
il campo magnetico sia uniforme
la traiettoria SbcC del fascio ionico (Fig. 50) che entra nel campo magnetico nel punto b ed
esce nel punto c per essere focalizzato nel collettore C, forma un angolo con lasse x ed
circolare nel tratto bc con un raggio R.
b
SS
yy
Oa
d
Fig. 50- Traiettoria del fascio ionico
Assumendo SO = OC = d :
da cui:
tag = y/p
p = (d-x)
tag = y/(d-x)
Dal triangolo abn si ottiene:
dato che:
La combinazione tra la (1) e la (2):
sen = x/R
sen /tag = cos
x/R
cos =
y /(d x)
(1)
(2)
(3)
40
Spettrometria di massa
Dal triangolo abn si ottiene anche:
cos = na/R
dove:
na R 2 x2
da cui:
cos =
Eguagliando la (3) e la (4):
x /R
R 2 x2
y /(d x)
R
che rielaborata d:
R2 x2
R
x(d x)
2
R x
(4)
(5)
Sostituendo nella (5) i diversi valori di R e di d per una certa SC fissa, si ottengono le coppie
di valori x e y che descrivono la forma del campo magnetico che consente la perfetta
focalizzazione di direzione. Negli spettrometri di massa la sezione approssimata del
magnete del tipo riportato nella Fig. 51.
Fig. 51- Sezione del magnete
4. LARGHEZZA DELLE FENDITURE
Le fenditure collegano la sorgente allanalizzatore e lanalizzatore al rivelatore. La loro
larghezza determina la quantit di ioni che attraversano i diversi settori dello spettrometro
di massa (Fig. 52). La larghezza delle fenditure viene modificata agendo sui sistemi
meccanici che sono comandati dalla consolle elettronica.
Fig. 52 Quantit di ion beam in funzione della larghezza delle fenditure
41
G. Bonaga
3.4.1. ANALIZZATORE MAGNETICO (Magnetic Analyzer = M)
Le soluzioni via via sempre pi pertinenti, che sono state messe a punto per risolvere i 4
problemi appena descritti, sono alla base del progresso e del successo degli analizzatori
magnetici. Con questi strumenti si pu effettuare la sola focalizzazione della direzione
mediante un settore magnetico (ANALIZZATORI A SINGOLA FOCALIZZAZIONE), od
anche la focalizzazione sia della direzione sia dellenergia cinetica mediante accoppiamenti,
realizzati in modo diverso, di un settore magnetico con un settore elettrostatico
(ANALIZZATORI A DOPPIA FOCALIZZAZIONE).
3.4.1.1.
SETTORE MAGNETICO
Gli ioni che vengono sottoposti allazione di un campo magnetico H, uniforme ed intenso,
seguono delle traiettorie circolari che, sebbene percorse in tempi differenti (tempo di volo),
hanno un raggio indipendente dalla massa dello ione. Dunque, campi magnetici uniformi non
separano ioni di massa differente. Nel 1933 Stephens dimostr lazione di lente di un settore
magnetico cuneiforme (Fig. 53).
Fig. 53 - Deflessione magnetica di ioni di m/z diversi
Gli ioni di massa m1 generati dalla sorgente S possono entrare nel settore magnetico H con
angoli di incidenza diversi. Con un angolo di 90 lo ione viene deflesso nel punto C1,
seguendo una curva di raggio r1; con un angolo minore di 90 lo ione verr sottoposto
allazione del campo per un tempo maggiore e verr pertanto deflesso nello stesso punto
C1, seguendo una curva di raggio maggiore r1; infine con un angolo maggiore di 90 lo
ione subir una deflessione su C1 secondo una traiettoria di raggio inferiore r1.
Naturalmente gli ioni di massa m2 verranno focalizzati in un punto C2 diverso da C1,
seguendo traiettorie di raggio r2 . Dunque, un settore a campo magnetico uniforme separa dal
fascio ionico, e focalizza nello stesso punto, pacchetti di ioni aventi lo stesso rapporto m/z e la
stessa velocit (sebbene direzioni differenti), ovvero separa e focalizza in punti diversi pacchetti di
ioni che hanno rapporti m/z e velocit differenti. Per gli ioni che emergono dalla sorgente, la
diminuzione dellenergia potenziale risulter uguale allaumento della loro energia cinetica:
zV
mv 2
2
(6)
lequazione rappresenta la repulsione elettrostatica.
42
Spettrometria di massa
Entrando in un campo magnetico uniforme essi diventano delle cariche in movimento, la
cui equazione del moto data dal bilancio tra il momento angolare e la forza centrifuga
prodotta dal campo:
mv 2
ovvero:
mv = Hzr
(7)
Hzv
r
lequazione rappresenta la deflessione magnetica.
Dalla combinazione delle equazioni (6) e (7) si ottiene:
m r 2 H2
z
2V
(8)
La (8) lequazione fondamentale della spettrometria di massa magnetica.
Essa indica la capacit di un campo magnetico uniforme H di separare degli ioni in base al loro
rapporto m/z e di focalizzarli in punti differenti, ma sottintende anche che facendo variare il campo
magnetico H (magnetic scan = scansione magnetica) ciascun gruppo di ioni aventi lo stesso
rapporto m/z viene focalizzato nello stesso punto in tempi diversi. (Con V in volts; v in
metri/secondo; H in gauss e r in centimetri; m risulter espresso in grammi e z in unit
elettrostatiche).
Lo schema di un analizzatore magnetico riportato nella Fig. 54.
Fig. 54 - Schema di uno spettrometro con analizzatore magnetico
3.4.1.2. SETTORE ELETTROSTATICO
Per ovviare alla disomogeneit delle energie cinetiche, gli ioni prodotti dalla sorgente ionica
vengono sottoposti allazione di un campo elettrostatico, prima (geometria normale) o dopo
(geometria inversa) essere stati sottoposti allazione di un campo magnetico. Come mostra
la Fig. 55, un campo elettrostatico radiale E , perpendicolare al campo magnetico H, viene
generato da due elettrodi di sezione cilindrica tra loro paralleli.
43
G. Bonaga
Fig. 55 - Traiettoria degli ioni in un campo elettrostatico
Gli ioni che entrano in questo settore elettrostatico vengono sottoposti allazione di una
forza centripeta che eguaglia la loro forza centrifuga:
E z = mv2/r1
(9)
Essendo la loro energia cinetica uguale allaccelerazione che subiscono per effetto del
potenziale V:
V z = mv2/2
(10)
la combinazione delle equazioni (9) e (10):
r1 = 2V/E
(11)
indica che gli ioni accelerati da un potenziale V e sottoposti allazione di un campo
elettrostatico E descrivono delle traiettorie circolari di raggio r 1, r2, ecc., indipendenti dalla
massa m.
Se E = costante si avr la focalizzazione di tutti gli ioni che hanno la stessa energia cinetica,
ovvero il campo elettrostatico funziona da filtro energetico in grado di garantire la
focalizzazione della velocit.
3.4.1.3. ANALIZZATORI A DOPPIA FOCALIZZAZIONE
Sono sistemi nei quali il fascio ionico viene sottoposto all'azione di un campo elettrostatico
E e di un campo magnetico H, tra loro perpendicolari e non sovrapposti, in modo da
ottenere sia la focalizzazione in energia che la focalizzazione in direzione. Sono possibili 2
geometrie: normale (Fig. 56a) e inversa (Fig. 56b).
44
Spettrometria di massa
a)
sorgente
ionica
settore
elettrostatico
1^ zona
di deriva
b)
sorgente
ionica
settore
magnetico
rivelatore
settore
elettrostatico
rivelatore
2^ zona
di deriva
settore
magnetico
Fig. 56 - Doppia focalizzazione a geometria normale (a) ed inversa (b)
Inizialmente la geometria normale (Fig. 57) consentiva una migliore risoluzione di massa ed
una relativamente pi elevata risoluzione energetica, ma successivamente si sono ottenuti
spettrometri di massa a geometria inversa (Fig. 58) con entrambe le risoluzioni pi elevate.
Fig. 57 - Spettrografo di massa di Mattauch-Herzog
Fig. 58 - Spettrometro di massa a geometria inversa ZAB a 2 fuochi
45
G. Bonaga
I numerosi elettrodi di allineamento situati lungo il percorso, consentono allo ZAB di
correggere la curvatura del fascio ionico; le 3 fenditure possono essere regolate sia in
larghezza che in altezza ed un secondo elettromoltiplicatore posto a 90 permette di usare lo
strumento sia a singolo che a doppio fuoco. Queste caratteristiche rendono possibile una
risoluzione di massa 100.000 ed una risoluzione energetica 5.000. Le alte prestazioni degli
analizzatori di quantit di moto sono dovute :
a)
b)
c)
d)
e)
elevatissima risoluzione;
massima sensibilit;
possibilit di misurare le masse esatte;
possibilit di rivelare gli ioni metastabili;
elevata velocit di scansione con i nuovi magneti laminari.
Queste prerogative fanno s che questi analizzatori siano i pi impiegati nel settore della
chimica strutturistica.
46
Spettrometria di massa
b) ANALIZZATORI DINAMICI
3.4.2. ANALIZZATORE QUADRUPOLARE (Quadrupole Analyzer = Q)
E' un analizzatore a stabilit di percorso che funziona come un vero e proprio filtro di
massa (Fig. 59).
Fig. 59 - Analizzatore quadrupolare
Tra le quattro barre di acciaio (rods), di sezione 6-15 mm e di lunghezza 10-30 cm, viene
creato un campo elettrodinamico quadrupolare (di radiofrequenza V e di corrente
continua U).
3.4.2.1. CAMPO QUADRUPOLARE
Il campo viene espresso in funzione della sua dipendenza lineare dalle coordinate spaziali:
E = E0 (x + y + z)
(12)
con , e costanti e con E0 funzione del tempo, ma indipendente dalla posizione.
47
G. Bonaga
Su uno ione sottoposto ad un campo quadrupolare agisce una forza zE che aumenta
allaumentare della distanza dallorigine. Il campo, invece, soggetto alle condizioni
imposte dallequazione di Laplace:
E=0
(13)
che corrisponde a: + + = 0
Per soddisfare lequazione si possono porre due valori:
= -; = 0 e = ; = -2
(14)
La forma del potenziale da applicare si ottiene dallintegrazione dellequazione (12):
1
E 0 (x 2 y 2 z 2 )
2
(15)
Imponendo le condizioni poste nella (14):
1
E0 (x 2 y 2 )
2
(16)
Le linee equipotenziali risultano essere un insieme di iperboli poste nel piano x-y, con
simmetria quadrilobata intorno all'asse z; un tale potenziale pu essere ottenuto con quattro
cilindri iperbolici i cui elettrodi adiacenti sono carichi di segno opposto (Fig. 60).
Fig 60 - Linee equipotenziali del campo quadrupolare e forma degli elettrodi
Se la distanza minima tra due elettrodi opposti 2r0 e il loro potenziale 0 , lequazione
(16) diventa:
0 (x 2 y 2 )
2r0
(17)
e quindi:
1
r02
In realt le barre di sezione circolare sono le pi approssimate rispetto quelle teoriche di
sezione iperbolica. Prendiamo in considerazione la forma del potenziale 0 , tenendo conto
che le equazioni di moto dello ione sono:
mx zE x
my zE y
mz zEz
48
Spettrometria di massa
Ricavando Ex,y,z dalla derivata della rispettiva dellequazione (17), si ottiene:
x (
) 0 x 0
mr02
z
y ( 2 ) 0 y 0
mr0
(18)
(19)
mz 0
Introducendo degli ioni nel campo quadrupolare, lungo la direzione dell'asse z, provvisti di
una certa velocit iniziale le equazioni (18) e (19) forniscono rispettivamente il moto dello
ione nei piani x-z e y-z.
Se i potenziali 0 = costanti, il moto risultante un semplice moto armonico nel piano x-z e
tutte le traiettorie risultano stabili, cio di ampiezza finita; soltanto nel piano y-z gli ioni
potrebbero divergere dall'asse z ed eventualmente neutralizzarsi sugli elettrodi.
Se i potenziali 0 = funzione periodica del tempo, le traiettorie degli ioni nei piani x-z e y-z
oscillano periodicamente lungo l'asse z, se si ammette una periodicit sufficientemente
ristretta e degli ioni abbastanza pesanti da non risentire della fase sfocalizzante del ciclo.
Se i potenziali 0 = costanti e periodici (combinazioni di V e U), gli ioni pi leggeri
avranno traiettorie instabili nella direzione x, lungo la quale saranno sottoposti ad
oscillazioni di ampiezza sempre crescente; la direzione x diviene quindi un filtro di massa
passa alto, dal momento che solo gli ioni di massa elevata attraversano il campo
quadrupolare senza urtare gli elettrodi. Gli ioni pi leggeri saranno, viceversa,
stabilizzati dalla componente alternata, che agisce nella direzione y, se lampiezza e la
frequenza sono tali da correggere le traiettorie; la direzione y diviene quindi un filtro di
massa passa basso. In definitiva, le direzioni x e y insieme sono un filtro di massa con un
passa banda determinato dalla combinazione tra la componente costante e quella
periodica.
Se, dunque:
0 U V cos t
con = frequenza, le equazioni (18) e (19) del moto dello ione diventano:
x (
y(
z
mr02
z
mr02
)(U V cos t)x 0
(20)
)(U V cos t)y 0
(21)
Definendo con:
au ax a y
q u q x q y
4zU
m 2 r02
2zV
m 2 r02
(22)
(23)
ed esprimendo il tempo in termini di periodo , le equazioni (20) e (21) assumono la stessa
forma:
d2 U
d 2
49
(a u 2q u cos 2 )u 0
(24)
G. Bonaga
dove u la coordinata x o y.
Lequazione (24) lequazione differenziale di Mathieu, un caso particolare dellequazione di
Hill:
d2 u
d 2
a 2q( )u 0
( ) ()
e quindi la (24) pu essere scritta:
d2 u
d 2
a u 2q u cos( 0 )u 0
Il parametro 0 il periodo iniziale, che tiene conto della fase del campo periodico quando lo
ione entra nel campo quadrupolare. Lequazione di Mathieu comporta delle soluzioni che
possono essere espresse dalla:
u e
C 2 n e 2 in e
C 2 n e 2 in
dove:
, = costanti di integrazione dipendenti dalle condizioni iniziali;
C2n, = costanti indipendenti dalle condizioni iniziali, ma dipendenti da a e da q.
Si pu quindi enunciare la prima propriet dellequazione di Mathieu:
la natura del moto degli ioni in un campo quadrupolare non dipende dalle condizioni iniziali, ma dai
valori di a e di q.
Poich dipende solo da a e da q, le condizioni di stabilit (per le quali rimane finito
per ) possono essere rappresentate con un diagramma di stabilit (Fig. 61) nel quale le
coordinate sono le stesse a e q (rispetto la coordinata generica u).
Fig. 61 - Diagramma di stabilit generica u nello spazio a,q
Passando da u alle coordinate reali x e y, le condizioni di una stabilit simultanea in
entrambe le direzioni x e y possono essere rappresentate con il diagramma di Fig. 62,
50
Spettrometria di massa
risultante dalla sovrapposizione dei due diagrammi di stabilit relativi a x e y che
differiscono di un fattore -1, come si pu dedurre dalle equazioni (22) e (23).
Limpiego, ad esempio, della prima regione di stabilit della Fig. 61 per ottenere la
risoluzione di massa, illustrato nella Fig. 63. Per valori fissati di r0, , U e V, tutti gli ioni di
uguale rapporto m/z hanno lo stesso punto operativo (a,q) nel diagramma di stabilit.
Poich:
a 2U
q
V
e non dipende da m/z, i punti operativi (il cosiddetto funzionamento) giacciono sulla stessa
retta del rapporto a/q = costante, che la linea di scansione di massa.
Fig. 62 - Diagramma di stabilit nelle direzioni x e y, nello spazio a,q
Fig. 63 - Prima regione di stabilit del diagramma di Fig. 61
Per a 0 solo ed esclusivamente gli ioni con punti operativi che giacciono allinterno della
regione di stabilit delle direzioni x e y possono attraversare il campo quadrupolare.
Aumentando il rapporto U/V varia il coefficiente angolare (1, 2, ecc.) della linea di
scansione di massa, che si avvicina sempre di pi allapice della prima regione di stabilit (R
= 1, R =10, ecc.) e soltanto un ristretto intervallo di valori m/z avr traiettorie stabili. Ioni di
massa minore saranno instabili nella direzione x e ioni di massa maggiore saranno instabili
51
G. Bonaga
nella direzione y. Per un determinato valore del rapporto U/V soltanto gli ioni di un solo
valore m/z attraverseranno il campo quadrupolare, mentre tutti gli altri andranno a
neutralizzarsi sugli elettrodi. Variando i valori di U e di V, pur mantenendo costante il loro
rapporto, oppure mantenendo U e V costanti e variando la frequenza, si pu effettuare la
scansione quadrupolare. La modulazione del campo elettrodinamico (radiofrequency scan
o quadrupole scan) consente di focalizzare sul rivelatore tutti i pacchetti di ioni aventi
diverso valore del rapporto m/z. La Fig. 64 mostra il passaggio attraverso il campo
quadrupolare di ioni a massa bassa e di ioni a massa alta, stabilizzati dai rispettivi rapporti
U/V lungo l'asse z.
Fig. 64 - Attraversamento del campo quadrupolare
Il range di massa e la risoluzione del campo quadrupolare dipendono dai seguenti
parametri:
range di massa
1. lunghezza delle barre
2. diametro delle barre
3. voltaggio massimo applicato alle barre
4. frequenza del campo RF
5. voltaggio di accelerazione degli ioni
risoluzione
La diffusione dellanalizzatore quadrupolare nel settore della chimica organica dovuta in
gran parte alla facilit di accoppiamento di questa tecnica di identificazione con tecniche di
separazione (GC-MS e LC-MS ed anche MS/MS) e/o con altre tecniche di identificazione
(FT-IR/MS, CE-MS). Questa facilit dipende proprio dalle caratteristiche peculiari
dellanalizzatore:
1. estrema semplicit e compattezza ;
2. elevata sensibilit (dellordine dei pg);
3. risoluzione (fino a 5.000) e range di massa (fino a 5.000 Da) sufficienti per la maggior
parte dei problemi analitici della chimica organica;
4. estrema velocit della scansione di RF (cycletime dellordine di 1 sec, per 1.000 Da);
5. ottenimento di spettri di massa in scala lineare anzich logaritmica;
6. tolleranza delle alte pressioni;
52
Spettrometria di massa
7. possibilit di rapide inversioni di campo, con conseguente ottenimento quasi simultaneo
degli spettri di massa di ioni positivi e di ioni negativi;
8. prezzo contenuto rispetto gli strumenti dotati di analizzatore magnetico.
I fattori che producono un abbassamento delle prestazioni di un analizzatore quadrupolare,
sono:
1. mancanza di allineamento delle barre: produce delle distorsioni del campo elettrodinamico
che determinano pessime separazioni degli ioni, con discriminazione degli ioni a basso,
medio ed alto valore del rapporto m/z;
2. contaminazione: lefficienza del filtro di massa dipende dalla stabilit dei voltaggi e delle
RF che governano lesattezza e lomogeneit del campo elettrodinamico; le impurezze
sulle barre, dunque, determinano delle variazioni di potenziale che fanno diminuire la
sensibilit (es: una variazione di circa 400 mV determina una diminuzione di sensibilit
del 4% circa);
3. forma delle barre: le superfici iperboliche ideali sono di difficile ottenimento e pertanto le
barre hanno sezione circolare e vengono disposte con un arrangiamento a quadrato per
ottenere la massima approssimazione del campo iperbolico; questa maggiore o minore
approssimazione incide sulle prestazioni dell'analizzatore.
3.4.3. ANALIZZATORE A TEMPO DI VOLO (Time of Flight = TOF)
E' un analizzatore che separa gli ioni esclusivamente in base alla loro diversa velocit. In un
analizzatore lineare pulsato a tempo si volo (Fig. 65), le molecole che provengono dalla
sonda portacampione si ionizzano in seguito allazione di un laser pulsato e gli ioni prodotti
vengono estratti per mezzo di un elettrodo estrattore (E1) a cui viene assegnata, ad
intermittenza, un potenziale negativo. La d.d.p. tra questo elettrodo e lelettrodo acceleratore
(E2), accelera gli ioni che, con una traiettoria rettilinea nel tratto E1 E3 (tubo di volo),
attraversano lelettrodo repulsore (E3) e vanno a colpire lelettrodo del rivetore (R). Al
rivelatore, per migliorare la separazione degli ioni, applicato un potenziale positivo dopo
che sono passati gli ioni di un certo m/z e prima che arrivino gli ioni del rapporto m/z
successivo.
Fig. 65 Analizzatore TOF
53
G. Bonaga
Gli ioni del fascio acquistano unenergia zV, cio pari alla carica dello ione (in unit
elettrostatiche) x potenziale di accelerazione, che uguale allenergia cinetica dello ione: zV
= 1/2mv2, da cui si pu ricavare il valore di:
1/v
m
2 eV
Per percorrere il tratto E1 R il tempo impiegato :
tv = d/v
d = distanza tra E1 e R e v = velocit dello ione. Sostituendo a 1/v il valore ricavato in
precedenza:
m
1m
tv
tv d
(con V e d = costanti)
2 Vz
z
Dunque, il tempo di volo direttamente proporzionale alla radice quadrata del rapporto
m/z.
ESEMPIO
Qual il tv degli ioni m/z 122 e m/z 105 ?
m/z 122 = 1105
m/z 105 = 1024
Nella Fig. 66 riportato lo spettro di massa TOF del C60 fullerene (mol wt 720).
Fig. 66 MS del fullerene 60
54
Spettrometria di massa
3.5. SISTEMI DI RIVELAZIONE DEGLI IONI
Esistono 4 tipi di rivelatori: il pozzo di Faraday, lelettromoltiplicatore, il deflettore elettrostatico e
la lastra fotografica. I primi due raccolgono i fasci ionici aventi diverso rapporto m/z,
amplificano i segnali e li trasmettono al registratore; il terzo rivela i fasci senza amplificarli
ed ha ormai valore esclusivamente storico, essendo stato il primo rivelatore montato sugli
spettrografi di massa.
Tutti gli attuali spettrometri di massa montano elettromoltiplicatori o fotomoltiplicatori che,
nonostante siano meno accurati del pozzo di Faraday, hanno una sensibilit molto
maggiore (fino a oltre 10-20A contro i 10-14A del pozzo di Faraday) ed una risposta molto
rapida, adatta al collegamento con lapparecchio di registrazione (oscilloscopio).
3.5.1. DEFLETTORE ELETTROSTATICO (ELECTROSTATIC DEFLECTOR = ED)
Il deflettore elettrostatico (Fig. 67) un sistema di rivelazione simultanea di tutte le specie
ioniche prodotte nella camera di ionizzazione. Una piastra a microcanali (accelerators grids)
collegata ad un deflettore elettrostatico in modo che il magnete sia in grado di separare gli
ioni in base:
a) al rapporto m/z;
b) alla velocit (v);
c) allangolo d'incidenza (traiettoria t).
L'impiego di questo rivelatore si diffuso specialmente nelle ricerche aerospaziali, dal
momento che gli ioni dello spazio possono essere catturati mediante una sonda ed inviati
direttamente al deflettore elettrostatico.
Fig. 67 - Rivelatore ED
55
G. Bonaga
3.5.2. ELETTROMOLTIPLICATORE (ELECTRONMULTIPLIER = EM)
E' costituito (Fig. 68) da un certo numero (10-20) di elettrodi metallici (comunemente Cu-Be)
curvi, detti dinodi, capaci di emettere facilmente elettroni secondari.
Fig. 68 - Rivelatore EM, preamplificatore, oscilloscopio
Il primo dinodo il collettore dei fasci ionici che escono dal settore dellanalizzatore,
attraversano la fenditura ed entrano nel settore del rivelatore; a potenziale negativo
(fino a circa -2000 V) e, per amplificare, deve avere un coefficiente di conversione elettroni
emessi/ioni incidenti > 1.
I successivi dinodi attraggono e focalizzano gli elettroni prodotti dal primo dinodo; essi
sono tenuti ad un potenziale progressivamente inferiore (per cui dal primo allultimo
dinodo c' una caduta di 1.500-2.000 V) ed hanno comunque coefficienti di conversione
sempre > 1. Lelettromoltiplicatore pu amplificare 106-108 volte una corrente in entrata
(variabile nellintervallo 10-11-10-19A) che determinata dal flusso ionico in entrata (la
microcorrente prodotta dal flusso di 1 ione/sec 10-19A)
Lultimo dinodo collegato ad un preamplificatore la cui funzione di applicare una
resistenza (103-109 ) alla corrente in uscita dallelettromoltiplicatore (variabile per effetto
dellamplificazione da 10-3-10-11A), in modo da ottenere un voltaggio di circa 100-10-2V
(pari a 10-1.000 mV) che un voltaggio compatibile con i galvanometri delloscilloscopio.
56
Spettrometria di massa
3.6. SISTEMI DI REGISTRAZIONE
OSCILLOSCOPIO
La corrente che proviene dal preamplificatore (Fig. 69) alimenta delle bobine mobili
(galvanometri a specchio) il cui angolo di deviazione proporzionale allintensit della
corrente che arriva nellelettromagnete. I raggi che provengono dalla lampada UV vengono
collimati sullo specchio del galvanometro, che provvede a riflettere ed imprimere sulla
carta fotosensibile un pennello di luce la cui altezza (od area) dipende dallangolo di
deviazione del galvanometro (ovvero dalla concentrazione della specie ionica che ha
prodotto una corrente di quella intensit).
In realt la connessione preamplificatore/galvanometri pi complessa perch viene realizzata
applicando sulla stessa corrente in uscita dallelettromoltiplicatore 3 resistenze ohmiche
diverse; si producono quindi 3 correnti di cui la seconda pari a 1/10 e la terza pari a
1/100 della prima. I tre diversi galvanometri che ricevono questi 3 segnali di diversa
intensit impressionano la carta fotosensibile nella quale appaiono, dunque, 3 tracce di
diversa sensibilit. Questo accorgimento consente un pi facile conteggio dei picchi ed
anche la misura delle altezze di quelli che hanno una scarsa abbondanza relativa.
Fig. 69 - Rivelatore EM, preamplificatore, oscilloscopio
57
G. Bonaga
3.7. POTERE RISOVENTE (RISOLUZIONE STRUMENTALE)
Lunit di massa atomica (a.m.u.) o il Dalton (Da) , attualmente, pari a 1/12 dell'isotopo 12C.
La scelta del peso dellatomo di C = 12,000000 determina in tutti gli altri atomi dei valori di
massa non interi, valori sempre pi in difetto con il crescere della massa (a causa
dellaumento della energia di legame nucleare). Le masse degli ioni dello spettro avranno
valori al massimo vicini, ma mai coincidenti con un numero intero.
Si prenda come esempio la serie di specie chimiche:
CO ; CH =N+ ; N ; C H
2
e si confrontino i valori corrispondenti alla massa approssimata (la massa dei chimici) con
quelli corrispondenti alla massa esatta (la massa dei fisici):
massa approssimata massa esatta
CO
CH2=N+
N2
C2H4
28
28
28
28
27,9949
28,0047
28,0061
28,0313
Nello spettro di massa della miscela di queste specie chimiche, ottenuto con spettrometri a
bassa risoluzione, sar visibile soltanto 1 picco al valore m/z 28, mentre nello spettro
registrato con uno spettrometro a media ed alta risoluzione si individueranno 4 picchi (Fig.
70).
Fig. 70 - Ioni molecolari nello spettro di massa ad alta risoluzione della miscela:
CO ; CH2=N+ ; N2 ; C2H4
Il potere risolutivo (o risoluzione) dunque la capacit di uno strumento di separare 2 ioni che
hanno massa [m] e [m + m].
Consideriamo (Fig.71) due ioni M1 e M2 che abbiano valori di massa che differiscono di M:
58
Spettrometria di massa
Fig. 71 - Risoluzione di due picchi M1 e M2
i due picchi vengono considerati separati se sono completamente risolti, ma anche se la loro
sovrapposizione (overlapping) limitata. Convenzionalmente sono separati quando
laltezza della valle tra i picchi (h) non supera il 10% della loro altezza (H).
h 10 % H
Il potere risolutivo o risoluzione (R) viene espresso perci dalla relazione:
R
M1
M
E' intuitivo che al crescere della massa degli ioni occorre una risoluzione R sempre pi
elevata. Per separare picchi che differiscono di 1 unit di massa occorre:
a) un basso potere risolvente a valori bassi (50-200) di a.m.u.;
b) un medio ed un elevato potere risolvente per valori medi (200-500) ed elevati (500-1500)
di a.m.u.:
M1 = 100
M1 = 500
M1 = 1.500
M = 1
M = 1
M = 1
R = 100/1 = 100
R = 500/1 = 500
R = 1.500/1 = 1.500
Alcune esempi ed applicazioni potranno chiarire ulteriormente linfluenza del potere
risolvente sulle prestazioni degli spettrometri di massa.
Esempio 1
Qual la risoluzione necessaria a separare i frammenti m/e 100 e m/e 101 ?
M1 = 100
M2 = 101
M = (101-100) = 1
R
59
M 1 100
100
M
1
G. Bonaga
Esempio 2
Qual la risoluzione necessaria a separare i frammenti m/e 500 e m/e 501 ?
M1 = 500
M2 = 501
M = (501-500) = 1
R
500
1
500
Esempio 3
Qual la risoluzione necessaria per separare il frammento CO+ dal frammento N 2 ?
CO 27,9949
N 2 28,0061
M = 0,01124
27 ,9949
0 ,01124
2.490
Esempio 4
Qual la risoluzione necessaria per separare degli ioni di m/e 135, ma che nelle
diverse combinazioni elementari possono differire a livello della terza cifra decimale ?
M = 135
M = 0,001
R
135
135.000
0 ,001
3.8. SENSIBILITA STRUMENTALE
La spettrometria di massa certamente la tecnica analitica pi sensibile, anche se il sistema
di introduzione del campione incide in modo rilevante sulla sensibilit effettiva dello
strumento:
a) Con il direct inlet i campioni vengono introdotti direttamente in sorgente e pertanto
linerzia del sistema garantisce la massima sensibilit spettrometrica, valutabile sulla base di
una intensit dello ione a m/z 298 generato da 1 pg (10-12 g) dello stearato di metile, che
deve essere 100 volte (i = 100) superiore alla linea di base (baseline) dello spettro.
Da due premesse: - resa in ioni (electron impact) = 1.10-6
- flusso molecolare in sorgente = 6.108 molecole/sec.
si pu dedurre:
- resa ionica (ioni/sec.) = 1.10-6 . 6.108 = 6.102 = 600
600 ioni/sec = quantit minima per registrare uno spettro di massa1
600 ioni/sec. producono allingresso dell'elettromoltiplicatore una corrente di I = 6 .10 17A.
60
Spettrometria di massa
Due esempi chiariranno limpiego di questi dati nel calcolo della sensibilit nella
spettrometria di massa.
Esempio 1
Calcolare se 1 pg di stearato di metile fornisce uno spettro di massa interpretabile.
CH3 (CH 2 )16 COOCH3
1pg
6 10 23
300 10 12
[mol wt = 298 300]
1 mole = 6.1023 molecole
2 10 9 molecole 1 10 6 2 10 3 ioni / sec
= 2000 = 2.000 ioni/sec
Esempio 2
Calcolare se 1 pg di tomidina fornisce uno spettro di massa interpretabile.
C50H83NO21 [mol wt = 1034 1000]
1pg
1 mole = 6.1023 molecole
6 10 23
6 10 8 molecole 1 10 6 6 10 2 ioni /sec = 600 ioni/sec
12
1000 10
b) Quando lo spettrometro accoppiato ad un sistema di introduzione dinamico (GC, LC,
ecc.), la diminuzione di sensibilit non prevedibile dal punto di vista teorico (dato il
grande numero di variabili che dipendono da un sistema di introduzione non inerte), ma
pu essere determinata mediante test nei quali la sensibilit viene espressa dal rapporto
tra il segnale fornito dagli ioni e il rumore dovuto al sistema dinamico (signal/noise =
S/N), naturalmente a valori definiti di risoluzione e di velocit di scansione. In generale,
uno spettrometro di massa accoppiato alla GC capillare, con sorgente EI, con analizzatore
magnetico e alla velocit di scansione di 1,5 sec/decade, fornisce un S/N 10 (i = 10) per lo
ione a m/z 298 generato da 100 pg di stearato di metile (10-10 g), cio con una sensibilit pari
ad 1/1.000 (102pg.101i ) di quella che si pu avere con lintroduzione diretta in sorgente.
61
G. Bonaga
4. LO SPETTRO DI MASSA
4.1. NORMALIZZAZIONE DELLO SPETTRO
L'introduzione di una sostanza nella sorgente ionica di uno spettrometro di massa produce
degli ioni positivi che derivano dalla ionizzazione delle molecole neutre e dalle successive
frammentazioni degli ioni molecolari pi o meno stabili che si sono formati. Gli ioni positivi,
accelerati da una d.d.p., collimati e focalizzati dalle lenti, costituiscono un ion beam che
entra nell'analizzatore di massa, nel quale vengono separati in base al valore del rapporto
m/z. I pacchetti di ioni aventi uguale rapporto m/z escono dallanalizzatore e vanno a
collidere con il collettore dellelettromoltiplicatore, producendo lemissione di elettroni
secondari; lamplificazione dei successivi dinodi d origine ad una corrente, sulla quale
viene applicata una resistenza ohmica che produce una corrente il cui voltaggio consente ai
galvanometri a specchio di tracciare sulla carta fotosensibile i segnali, detti picchi, le cui
altezze rivelano labbondanza degli ioni che li hanno originati.
Il risultato di questa registrazione lo spettro di massa reale, nel quale occorre procedere
allassegnazione dei valori del rapporto m/z sullasse delle ascisse e alla misurazione delle
abbondanze dei differenti valori m/z sullasse delle ordinate.
4.1.1. CONTEGGIO (assegnazione dei valori m/z)
Negli spettri di massa reali con analizzatore magnetico, la scala dei valori m/z logaritmica
e pertanto gli intervalli tra i picchi degli ioni sono progressivamente minori procedendo
dalle masse basse verso le masse alte. Questo conteggio manuale si pu avvalere della
identificazione, pi facile, di alcuni valori m/z caratteristici, come quelli dovuti alla
presenza di tracce di aria e vapore dacqua nella sorgente ionica dello spettrometro. Essi sono:
H2O+ = m/z 18; N2+ = m/z 28; O2+ = m/z 32; Ar+ = m/z 40 e CO2+ = m/z 44
Qualora il conteggio fosse problematico alle masse medie ed alte, si pu procedere alla
registrazione di spettri di massa di standard di cui siano noti e facilmente identificabili certi
valori di m/z (ad es.: perfluorokerosene, terz-[nonafluorobutil]ammina, ecc.). La Fig. 72 mostra
lo schema di frammentazione della terz-[nonafluorobutil]ammina, i cui picchi caratteristici
consentono, oltre al conteggio dello spettro, la calibrazione dello spettrometro di massa
(messa a punto delle migliori condizioni di sensibilit e di risoluzione).
Fig. 72 - Frammentazione della terz-[nonafluorobutil]ammina (FC43)
62
Spettrometria di massa
Gli spettrometri di massa attuali sono dotati di mass marker, dispositivi che stampano
sullo spettro degli intervalli prestabiliti di unit di massa (in genere 10), allinterno dei quali
pi facile lidentificazione dei valori m/z.
bobina
rotante
100
segnale
S
Fig. 73 - Mass marker a bobina rotante
Nel caso della bobina rotante tra le espansioni polari di un magnete (Fig. 73) per ogni valore
del campo magnetico verr indotta una forza elettromotrice (f.e.m.) agli estremi della
bobina. Digitalizzando i valori della f.e.m. si pu risalire al valore di m/z focalizzato dal
magnete, che viene mostrato nella fenditura del collettore (nella figura: m/z = 100). Un altro
tipo di mass marker impiega un cristallo semiconduttore sempre tra le espansioni polari di
un magnete; la conducibilit del semiconduttore varia al variare del campo magnetico in
accordo con leffetto Hall, quindi digitalizzando i valori della conducibilit si possono
tarare i valori m/z. Essendo un dispositivo meccanico ed elettronico, il mass marker ha una
precisione che dipende molto dalla sua efficiente taratura, operazione che viene fatta con
una certa frequenza impiegando standard di rifermento che forniscono spettri di facile
interpretazione.
4.1.2. ABBONDANZA DEGLI IONI
La misura delle abbondanze dei diversi picchi (absolute intensity) si esegue misurando
laltezza dei segnali ai diversi valori m/z (oppure calcolando la corrente ionica di ciascun
ione rispetto la corrente ionica totale).
4.1.3. NORMALIZZAZIONE DELLO SPETTRO
Se si riportano su scale lineari i valori m/z e le corrispondenti abbondanze relative, (relative
intensity), cio riferite al picco pi intenso dello spettro posto = 100 (detto picco base =
base peak), si ottengono gli spettri di massa normalizzati. La conversione dello spettro reale in
spettro normalizzato, fatta esclusivamente in modo manuale nei primi anni della
spettrometria di massa, viene effettuata dal convertitore analogico-digitale del computer, che
ormai interfacciato in tutti gli spettrometri moderni, sia magnetici che quadrupolari. Il
convertitore trasforma i segnali codificati da un sistema binario (binary digit) in segnali
digitali corrispondenti alla posizione e allintensit dei picchi dello spettro. Nelle Fig. 74 e 75
sono riportati, rispettivamente, lo spettro normalizzato e quello reale (in tre scale di sensibilit)
dellanilina.
63
G. Bonaga
Fig. 74 - Spettro di massa normalizzato dell'anilina
Fig. 75 - Spettro di massa reale dellanilina in tre scale di sensibilit
4.2. PARTICOLARITA DELLO SPETTRO DI MASSA
E necessario premettere che:
negli SPETTROMETRI A BASSA RISOLUZIONE il valore m del rapporto m/z
rappresenta la massa nominale dello ione, cio il numero intero pi vicino alla massa
dovuta agli isotopi pi abbondanti degli elementi presenti nello ione.
es.:
CH3-OH+. = m/z 32
negli SPETTROMETRI AD ALTA RISOLUZIONE il valore m rappresenta la massa
esatta dello ione, cio il numero di massa esatto dovuta agli isotopi degli elementi
presenti nello ione.
es.:
CH3-OH+. = m/z 32,026214
Soltanto con gli spettrometri di massa ad alta risoluzione si pu, dunque, individuare la
composizione elementare degli ioni e, nel caso lo ione molecolare sia abbastanza stabile, anche
la composizione elementare della molecola.
64
Spettrometria di massa
4.2.1. IONE MOLECOLARE
Nella Ms a ioni positivi in realt un radical-ione [M]+. che si forma per ionizzazione delle
molecole neutre. Se sufficientemente stabile sar visibile sullo spettro al valore pi elevato
di m/z (escludendo eventuali impurezze di peso molecolare superiore a quello dellanalita).
Nei prossimi paragrafi verranno presi in considerazione tutti i fattori che governano la
formazione, la stabilit e la frammentazione dello ione molecolare; per ora sufficiente
ricordare che la sua individuazione consente di conoscere la massa nominale (MS a bassa
risoluzione) o la massa esatta (MS ad alta risoluzione) della molecola. Nella registrazione
degli spettri di massa a 70 eV, per, soltanto il 20% circa dei composti organici fornisce degli
ioni molecolari abbastanza stabili da produrre un segnale registrabile. La Fig. 76 riporta la
struttura dello ione molecolare dellacido benzoico.
+.
.
Fig. 76 Struttura del C6H5-COOH
4.2.2. IONI MULTIPLI
La maggior parte degli elementi presenti nei composti organici sono costituiti da diversi
nuclidi, come si deduce dalla Tabella 1. Questa particolarit determina la comparsa, negli
spettri, di picchi multipli ovvero gruppi di valori m/z che differiscono di 1, 2, 3, 4, ecc.
a.m.u.
Tabella 1 - Masse e composizioni isotopiche di elementi comuni delle molecole organiche
65
ELEMENTO
PESO
ATOMICO
idrogeno
1,00797
carbonio
12,01115
azoto
14,00670
ossigeno
15,99940
fluoro
18,99840
silicio
28,08600
fosforo
30,97380
zolfo
32,06400
cloro
35,45300
bromo
79,90900
iodio
126,90400
NUCLIDI
1H
2H
12C
13C
14N
15N
16O
18O
19F
28Si
29Si
30Si
31P
32S
33S
34S
35Cl
37Cl
79Br
81Br
127I
MASSA
ESATTA
1,007825
2,014102
12,000000
13,003354
14,003074
15,000108
15,994915
17,99916
18,998405
27,976929
28,976492
29,973758
30,973764
31,972073
32,971463
33,968853
34,968851
36,965903
78,918329
80,916344
126,904662
% ABBONDANZA % ABBONDANZA
ASSOLUTA
RELATIVA
99,99
100
0,01
0,016
98,9
100
1,1
1,08
99,6
100
0,4
0,36
99,8
100
0,2
0,19
100
100
92,2
100
4,7
5,07
3,1
3,31
100
100
95
100
0,7
0,78
4,2
4,39
75,5
100
24,5
32,7
50,5
100
49,5
97,5
100
100
G. Bonaga
Nella spettrometria di massa i casi pi importanti riguardano: carbonio, cloro, bromo, zolfo.
CARBONIO
In un composto che contiene 1 solo atomo di C (CH4), la probabilit che sia presente 13C
dell1,1%, ma in un composto che contiene 6 atomi di C (C6H5-NH2) la probabilit diventa
(1,1 x 6) del 6,6% (Fig.77).
Fig. 77 - Picchi corrispondenti agli ioni M e M+1 negli spettri del metano e dellanilina
Sono disponibile delle tavole isotopiche che riportano i contributi dei diversi nuclidi M+1,
M+2, M+3, M+4, ecc. Negli spettri di massa, dunque, i composti del carbonio mostrano il
gruppo isotopico M, M+1 e M+2, corrispondente alle combinazioni 12C12C, 12C13C, 13C13C.
Le altezze relative dei picchi M e M+1 possono fornire, nei casi pi favorevoli, il numero di
atomi di carbonio presenti negli ioni, sia in quelli molecolari che negli ioni frammento.
N atomi di C =
%M 1
1 ,1
Il numero che si ottiene attendibile se:
1. gli atomi di C presenti nello ione non sono pi di 12;
2. lo ione molecolare non viene protonato con facilit (come succede negli alcoli, esteri, acidi,
nitrili, amminoalcoli, amminoesteri,ecc.)
CLORO
Lintensit relativa dei multipletti dovuti ai nuclidi del cloro si ottiene dallo sviluppo
del binomio:
(a+b)n
a) Il cloruro di vinile contiene 1 solo atomo di cloro, ma sono presenti due specie
isotopicamente diverse, una contenente 35Cl e una contenente 37Cl, nel rapporto 3:1
risultante dalla risoluzione del binomio (0,75+0,25)1. Lo spettro del composto (Fig. 78a)
mostra infatti la coppia di ioni molecolari isotopici a m/z 62 e 64 nel rapporto 3:1.
b) Nell1,4-diclorobenzene, i 2 atomi di cloro danno origine ad un tripletto con
abbondanze che risultano dallo sviluppo del binomio: (a+b)2 = 9:6:1. Lo spettro del
composto (Fig. 78b) mostra infatti un tripletto dovuto alle formule isotopiche 35Cl 35Cl, 35Cl
37Cl, 37Cl 37Cl, i cui rapporti rispettano i valori teorici.
66
Spettrometria di massa
Fig. 78 - Spettri di massa del cloruro di vinile e dell1,4-diclorobenzene
c) Nel caso del cloroformio (Fig. 79) le stesse considerazioni spiegano la presenza di un
quadripletto isotopico.
Fig. 79 - Spettro di massa del cloroformio
d) Anche nel caso del tetracloruro di carbonio (Fig.80) il quintupletto e i rapporti
isotopici relativi si giustificano in modo analogo.
Fig. 80 - Spettro di massa del tetracloruro di carbonio
BROMO
Anche l'intensit relativa dei multipletti dovuti ai nuclidi del Br si ottiene dallo
sviluppo del binomio:
(c+d)m
67
G. Bonaga
a) Nel caso del bromuro di vinile (Fig. 81a) gli ioni molecolari isotopici a m/z 106 e a
m/z 108 sono presenti, come prevedibile, in un rapporto approssimativamente = 1:1.
b) Anche i picchi multipli dell1,4-dibromobenzene (Fig. 81b) hanno una interpretazione
analoga.
Fig. 81 - Spettri di massa del bromuro di vinile e dell1,4-dibromobenzene
c) Lo spettro del bromoformio (Fig.82) pu essere interpretato in modo analogo.
Fig. 82 - Spettro di massa del bromoformio
CLORO E BROMO
In una molecola che contiene atomi di cloro e atomi di bromo, la combinazione e la
distribuzione isotopica negli ioni si ottengono dalla risoluzione del prodotto dei binomi
relativi al cloro (a e b) e al bromo (c e d):
(a+b)n x (c+d)m
a) Il diclorodibromoetano mostra uno spettro (Fig. 83) con cinque picchi molecolari che
corrispondono alle 9 distribuzioni isotopiche deducibili dalle possibili
combinazioni del prodotto dei due binomi.
68
Spettrometria di massa
Fig. 83 - Spettro di massa (parziale) del diclorodibromoetano
Gli ioni a m/z 255, 257, 259, 261 e 263, peraltro appena percettibili, sono i picchi isotopici
dovuti al 13C.
ZOLFO
Mentre sono di grande utilit diagnostica gli isotopi dello zolfo dello ione
molecolare, nei frammenti la presenza dello zolfo viene di frequente mascherata da altri
ioni frammento privi di zolfo. Negli ioni frammento sono pi importanti, invece, le perdite
caratteristiche di 32, 33 e 34 a.m.u.
a) Lo spettro delletilmercaptano (Fig.84) mostra il doppietto dei 2 ioni molecolari
isotopici ed anche alcuni frammenti caratteristici ([M+- 15], [HCS+], ecc.).
Fig. 84 - Spettro di massa delletilmercaptano
69
G. Bonaga
4.2.3. IONI METASTABILI
Dalla Fig. 85 si pu dedurre che gli ioni formati nella sorgente emergono dalla fenditura ed
entrano in un campo di potenziale (AB) che li accelera verso il campo magnetico (CD).
Fig. 85 - Formazione di ioni metastabili
Nel cammino che essi percorrono soltanto il tratto BC privo di campo; se uno ione ( m 1 ) si
frammenta nel tratto BC (tenendo conto che la vita media degli ioni di 5-10 s e il tempo
medio per percorrere il tratto AD di circa 10-15 s), lenergia cinetica ricevuta dal campo
di accelerazione si ripartisce tra lo ione che si genera ( m 2 ) e la particella neutra (pn) che
viene espulsa. Dunque, lo ione figlio ( m 2 ) entra nel settore magnetico con unenergia
traslazionale minore di quella che avrebbe ricevuto nel settore elettrostatico e pertanto
subisce una deviazione maggiore dal campo magnetico; il risultato che questo ione viene
rivelato e registrato ad un valore m/z inferiore a quello che gli competerebbe. Si tratta di
una transizione metastabile:
*
m 1 m 2 pn
che produce uno ione metastabile m*, la cui posizione nello spettro data dalla relazione:
m*
m 2
m 1
Questa relazione la conseguenza stessa dellapplicazione delle equazioni fondamentali
della spettrometria di massa magnetica:
mv2
mv2
Hzv
zV
(25)
(26)
r
2
Applicando la (25) allo ione-padre m1 si ha:
mv2
zV 1 1
da cui:
2
v1
2zV
m1
(27)
70
Spettrometria di massa
Nella zona priva di campo lo ione-figlio m 2 , che si forma per la transizione metastabile,
viaggia verso il settore magnetico con la stessa velocit v1 dello ione-padre m 1 ; esso subir
pertanto una deflessione magnetica deducibile dalla (26):
m1 v12
Hzv1
r
Sostituendo a v1 il valore trovato con la (27):
2zV
Her
m1
m22
m22 2zV
H2 z2 r 2
m1
da cui:
risolvendo:
m22 H 2 z 2 r 2
m1
2zV
m 22 H 2 r 2
m1
2V
z
da cui:
Questa equazione sempre lequazione fondamentale della spettrometria di massa
magnetica, ma adattata ad uno ione frammento che si forma nel tratto privo di campi. I
picchi metastabili sono dunque picchi tipici della spettrometria di massa magnetica; essi
appaiono sullo spettro con forma allargata, schiacciata e asimmetrica, ma la loro grande
importanza dovuta al fatto che consentono di individuare o confermare le perdite di
frammenti neutri.
Vengono riportati 2 esempi: anilina e acetofenone
ANILINA (mol wt 93)
in sorgente:
picco nello spettro
M+e
M+. + 2e
m/z 93
M+.
(M HCN) +.
m/z 66
M+.
(M HCN) +.
m/z 46,8
nel tratto BC:
(m* = 662/93 = 46,8)
ACETOFENONE (mol wt 120)
in sorgente:
picco nello spettro
M+e
M+. + 2e
m/z 120
M+.
(M 15) +
m/z 105
(M 15) +
(M 15 - CO) +
m/z
77
(M 15) +
(M 15 - CO) +
m/z
56,5
nel tratto BC:
(m* = 772/105 =56,5)
71
G. Bonaga
4.2.4. IONI A CARICA MULTIPLA
Sono dovuti allestrazione di 2 o 3 elettroni della molecola da parte dellelettrone
bombardante (sorgenti EI):
M + e- M++ + 3eM + e- M+++ + 4eGli ioni a tripla carica sono improbabili perch l'energia di 3^ ionizzazione estremamente
elevata, mentre quelli a doppia carica sono caratteristici dei composti aromatici, nei quali
lanello aromatico delocalizza bene le due cariche positive.
Negli spettrometri a bassa risoluzione gli ioni a carica multipla sono utili per confermare il
valore della massa nominale dello ione molecolare, dal momento che essi sono
sottomultipli interi e non interi della massa degli ioni molecolari a carica singola; oltre a
confermare il carattere aromatico dei composti servono anche nellassegnazione dei valori
m/z nel conteggio manuale dei picchi dello spettro. Nella Fig. 86 sono riportati 3 esempi:
anilina, fenolo e aldeide benzoica.
ANILINA
FENOLO
ALDEIDE BENZOICA
Fig. 86 - Ioni a doppia carica di anilina, fenolo e aldeide benzoica
72
Spettrometria di massa
4.2.5. FRAMMENTI CARATTERISTICI
Negli ioni possibilie individuare la presenza di atomi di ossigeno e di azoto, attraverso lo
studio di alcune frammentazioni caratteristiche.
OSSIGENO
La presenza dellossigeno si pu dedurre sulla base di perdite caratteristiche di specie
neutre (molecole o radicali) dallo ione molecolare:
M - 18 : perdita di
M - 28 : perdita di
M - 31 : perdita di
M - 45 : perdita di
M - 59 : perdita di
H2 O
CO
.OCH3
.COO
.COOCH3
AZOTO
Lazoto lunico elemento ad avere peso atomico pari (14) e valenza dispari (3), pertanto un
numero dispari di atomi di N produrr un numero dispari m/z dello ione molecolare; la
presenza dellazoto si pu dedurre anche dalle perdite caratteristiche di specie neutre
(molecole o radicali) dallo ione molecolare:
M - 27 : perdita di HCN
M - 16 : perdita di .NH2 (solo nelle ammidi)
4.2.6. CALCOLO DELLE INSATURAZIONI E/O DEGLI ANELLI
Se, attraverso la spettrometria ad alta risoluzione oppure tramite linsieme delle deduzioni
che sono state appena fatte, si determinata la composizione elementare della sostanza
presa in esame:
CxHyNzOn
Se si inglobano in C tutti gli elementi tetravalenti (silicio), in H quelli monovalenti (alogeni),
in N quelli trivalenti (fosforo) ed in O quelli bivalenti (zolfo), si pu calcolare il numero
complessivo delle insaturazioni e/o degli anelli presenti nella sostanza:
1
1
n insaturazioni e/o anelli = x y z 1
2
2
Sono riportati 2 esempi: il nitrobenzene (a) e il 4-(1-propen-1-il)acetofenone (b):
1
1
2
2
1
b) C11H12 O2 11 12 1 6
2
a) C6 H5 NO2 6 5 1 1 5
73
(4 insaturazioni + 1 anello)
(5 insaturazioni + 1 anello)
G. Bonaga
5. FORMAZIONE E DECOMPOSIZIONE DELLO IONE MOLECOLARE
La spettrometria di massa dei composti organici si sviluppa su due direttici:
1. deduzioni strutturali del composto analizzato (formula molecolare e struttura);
2. interpretazione razionale dello schema di frammentazione del composto.
In entrambi i casi non si pu prescindere dalla interpretazione logica dello spettro, che
viene fatta tenendo conto delle conoscenze teoriche e dei risultati sperimentali che si sono
consolidati nel tempo.
Verranno presi in considerazione gli aspetti teorici qualitativi e quantitativi pi importanti
nella formazione dello ione molecolare e nelle successive frammentazioni:
Formazione e stabilit dello ione molecolare
Decomposizione (o frammentazione) dello ione molecolare
Fattori che governano la decomposizione
Produzione di frammenti
Reazioni ioniche
5.1. FORMAZIONE E STABILITA DELLO IONE MOLECOLARE
Nella ionizzazione per EI, la produzione dello ione molecolare richiede lestrazione di un
elettrone da un orbitale molecolare dellanalita. La maggior parte delle molecole organiche
richiedono unenergia compresa tra 7-13 eV (pari a 150-300 kcal/mole). Questa energia
detta energia di ionizzazione (ionization energy = IE) - viene fornita in modo diverso secondo
il tipo di sorgente ionica. Nel caso delle sorgenti EI un fascio di elettroni emesso da un
filamento di renio riscaldato a circa 300C ed accelerato da una d.d.p. di 10-70 V, a
determinare la ionizzazione. Questi elettroni possono trasferire alla molecola unenergia di
10-70 eV. Ai valori di pressione della sorgente ( 10-7 torr) il cammino libero delle molecole
di cerca 20 centimetri e pertanto le collisioni tra molecole neutre e ioni sono estremamente
improbabili. Se lo ione molecolare si decompone, il processo dunque monomolecolare.
Daltra parte, lenergia di comparsa (appearance energy = AE) di uno ione lenergia
minima richiesta per la sua formazione; solo nel caso dello ione molecolare lenergia di
comparsa coincide con la sua energia di ionizzazione. Lo ione molecolare, dunque, possiede
unenergia totale (E) risultante dalla somma dellenergia termica (Et) dovuta al calore della
sorgente ionica (300C 3 eV) e dellenergia dellelettrone collidente (Eel):
E = Et + Eel
se:
E IE
E >> IE
lo ione molecolare pu non decomporsi ed apparire nello spettro;
lo ione molecolare si decompone e raramente appare nello spettro.
Le due relazioni indicano genericamente che, ammessa una certa stabilit dello ione
molecolare, lenergia degli elettroni dell electron beam determinante nel causare o no la
decomposiziome dello ione molecolare. Limpiego di elettroni collidenti a 20 eV, pertanto,
uno dei mezzi per ottenere spettri di massa nei quali lo ione molecolare, se sufficientemente
stabile, risulta pi visibile. La considerazione non ha valore assoluto perch la maggior
parte dei composti organici non d ioni molecolari stabili (ad es., tra quelli di peso
molecolare attorno a 600 a.m.u. soltanto il 20% circa fornisce ioni molecolari stabili) dal
74
Spettrometria di massa
momento che le energie di attivazione delle reazioni di decomposizione degli ioni
molecolari sono spesso molto basse.
Sia pure approssimativamente, le principali classi di composti organici mostrano
un'abbondanza degli ioni molecolari che pu essere, con buona approssimazione, cos
riassunta:
ABBONDANZA DI M+.
100-50%
Idrocarburi aromatici
Eterociclici aromatici
Cicloalcani
R-SH
R-S-R
Ar-F
Ar-Cl
Ar-CN
Ar-NH2
50-10%
Alcheni
Ammidi
Chetoni
Aldeidi
Eteri
Ar-Br
Ar-I
Ar-CO-R
10-0%
Alcani
Esteri
Alogenuri alchilici
Alcoli alifatici
Nitrili alifatici
5.2. DECOMPOSIZIONE DELLO IONE MOLECOLARE
La decomposizione dello ione molecolare non casuale, ma voluta, nel senso che leccesso
di energia trasferita alla molecola iniziale dagli elettroni collidenti (nel caso di sorgenti EI)
ha proprio lo scopo di favorire la frammentazione dello ione molecolare che si forma per
ionizzazione. Linsieme delle reazioni che avvengono nella sorgente ionica pu essere cos
riassunto, tenendo conto della seguente simbologia:
[ep] = molecola neutra ad elettroni pari
[ed] +. = radicale-ione ad elettroni dispari
[ed] . = radicale ad elettroni dispari
[ep]+ = ione ad elettroni pari
1. REAZIONE DI IONIZZAZIONE
[ep] + e- [ed] +. + 2e[ep] + e- [ed]++ + 3e-
( [ed]+. = M+.)
( [ed]++ = M++ )
2. REAZIONI DI DECOMPOSIZIONE PRIMARIA
a.
[ed] +. [ep]+ + [ed]. reazione di scissione
b.
[ed] +. [ed]+. + [ep] reazione di trasposizione
3. REAZIONI DI DECOMPOSIZIONE SECONDARIA
c.
[ed] +. [ep]+ + [ed]. reazione di scissione
d.
[ed] +. [ed] +. + [ep] reazione di trasposizione
e.
[ep]+ [ep]+ + [ep]
f.
[ep]+ [ed]+. + [ed].
4. REAZIONI IONE-MOLECOLA
g.
[ed] +. + [ep] [ep]+ + [ed].
h.
[ed] +. + [ed]. [ep]+ + [ep]
75
G. Bonaga
Dallo ione molecolare si hanno reazioni di decomposizione primaria che, nel rispetto del
principio di conservazione della carica, producono:
a) uno ione monocarico [ep]+ e un radicale [ed]. oppure;
b) radicale-ione monocarico [ed]+. e una molecola neutra [ep].
Gli ioni a elettroni pari sono pi stabili degli ioni a elettroni dispari e pertanto avranno
unabbondanza superiore nello spettro di massa; gli ioni che si formano nei processi di
decomposizione primaria possono, se hanno sufficiente energia interna, decomporsi
ulteriormente secondo reazioni di decomposizione secondaria, dalle quali si ottengono ioni,
radicali-ioni, radicali e molecole neutre, fino alla produzione di ioni che non si
decompongono. Una decomposizione che produce anche lo spostamento di atomi si
definisce trasposizione (rearrangement reaction), mentre se lo ione molecolare reagisce con
una molecola neutra o con un radicale (processo peraltro improbabile ai valori di pressione
della sorgente ionica) si ottiene una specie chimica detta ione quasi-molecolare, cio uno
ione a numero pari di elettroni, ma con una o pi unit di massa atomica (per cattura o
perdita di uno o pi atomi di idrogeno o di altri ioni). Questo comportamento frequente
nelle molecole contenenti gruppi polari: esteri, eteri, ammine, ammino-esteri, nitrili, ecc.). Gli
ioni quasi-molecolari sono lobiettivo delle ionizzazioni soft, oggi molto utilizzate (ESI,
APCI, MALDI, FAB).
5.3. FATTORI CHE GOVERNANO LA DECOMPOSIZIONE
Considerando la complessit dei processi che avvengono nella sorgente ionica, necessario
rispondere ad alcune domande. Tra tutte le reazioni possibili, quali sono le pi probabili e
quali fattori ne governano lo svolgimento ?
I fattori fondamentali sono 2:
a) fattore energetico;
b) fattore cinetico.
5.3.1. FATTORE ENERGETICO
Gli elettroni che collidono con le molecole neutre trasferiscono ad esse quantit differenti di
energia, sebbene leffetto principale la loro ionizzazione.
Nelle sorgenti, quindi, si forma una collezione di ioni molecolari a diversa energia interna
(energia termica + energia elettronica) che si decompongono in ioni di frammentazione a
differente energia di comparsa. Questo fatto spiega perch nelle sorgenti EI si utilizza un
energia di 70 eV; con questa energia, infatti, gli spettri di massa non solo mostreranno tutti i
tipi di decomposizione, ma saranno riproducibili anche se ottenuti con strumenti diversi.
La relazione tra energia di ionizzazione (IE) ed energia di comparsa (AE) :
AE - IE = Eatt
Lenergia di attivazione (Eatt) dunque necessaria ad innescare una decomposizione ionica
ed la prima risposta alla domanda iniziale: tra le varie reazioni di decomposizione le pi
probabili sono quelle che richiedono la minore energia di attivazione
Dal punto di vista energetico i processi di ionizzazione dovrebbero avere il seguente ordine
di probabilit:
PROBABILIT' DI FORMAZIONE DEGLI IONI IN TERMINI ENERGETICI (70 eV)
reazioni di I^ ionizzazione > reazioni di trasposizione > reazioni di scissione > reazioni di II^ ionizzazione
76
Spettrometria di massa
La curva di efficienza di ionizzazione della piridina (Fig.87) dimostra leffetto dellenergia
degli elettroni collidenti sulla resa in ioni.
Fig. 87 - Curva di efficienza di ionizzazione della piridina
5.3.2. FATTORE CINETICO
Labbondanza di uno ione di decomposizione dipende anche dalle velocit delle reazioni
che precedono la sua formazione e dalle velocit delle reazioni che la seguono. A 70 eV
sono pi veloci le reazioni di scissione rispetto le reazioni di trasposizione, anche se le
scissioni richiedono unenergia maggiore.
La combinazione del fattore energetico con quello cinetico danno lordine reale delle
reazioni che avvengono allinterno della sorgente ionica:
PROBABILIT' REALE DI FORMAZIONE DEGLI IONI (70 eV)
reazioni di I^ ionizzazione > reazioni di scissione > reazioni di trasposizione > reazioni di II^ ionizzazione
Gli effetti sullo spettro di massa delle effettive probabilit si possono cos riassumere:
1. lo ione molecolare sar sufficientemente abbondante se la sua struttura sufficientemente
stabile;
2. nella zona delle masse alte prevarranno gli ioni generati da reazioni di scissione;
3. nella zona delle masse basse e medie prevarranno gli ioni generati da reazioni di
trasposizione;
4. nella zona delle masse basse prevarranno gli ioni stabili che non si decompongono;
5. nella zona media dello spettro potranno comparire gli ioni a doppia carica (mezze masse).
5.4. PRODUZIONE DI FRAMMENTI
5.4.1. TEORIA DELLA FRAMMENTAZIONE
Per interpretare gli spettri di massa occorre conoscere nei dettagli la natura dei processi che
avvengono nella sorgente ionica. Mentre nel corso di una reazione chimica il reattivo
attacca una parte specifica della molecola (il fattore di orientamento della cinetica chimica),
nellinterazione elettrone-molecola lelettrone, relativamente piccolo, molto energetico (70
eV 1500 kcal/mole) ed estremamente veloce (105Km/s), pu collidere con ogni parte
della molecola.
77
G. Bonaga
Se tutta l'energia dellelettrone fosse trasferita alla molecola si romperebbero tutti i legami
chimici, dal momento che lenergia media di legame di 75 kcal/mole. In questo modo si
produrrebbero ioni ed atomi singoli di qualit e in quantit cos elevate che ogni
correlazione tra struttura della molecola e tipo di ioni prodotti sarebbe difficile.
Fortunatamente il trasferimento di energia dallelettrone alla molecola neutra solo
parziale; lenergia non rimane localizzata in un punto della molecola e pertanto lo ione che
viene prodotto non si dissocia di colpo, ma ha un tempo finito di vita.
Nel gran numero di molecole presenti:
a) una parte assorbe energia pari a circa 7-11 eV, che corrisponde allintervallo del
potenziale di ionizzazione dei principali composti organici,
b) unaltra parte assorbe delle quantit di energia leggermente superiori alle probabilit di
transizione fra molecola neutra e ione molecolare, di 5-6 eV superiori ai potenziali di
ionizzazione.
In questo modo si ottiene una popolazione di ioni molecolari in stati energetici differenti,
ciascuno dei quali si comporter come entit separata in relazione alla quantit specifica di
energia in eccesso che possiede.
Questo processo pu essere rappresentato con la curva della distribuzione dellenergia
degli ioni molecolari dellacido benzoico, illustrata nella Fig. 88.
Lenergia coinvolta nella ionizzazione semplice dellacido benzoico compresa
nell'intervallo 9,7-12,7 eV; gli ioni molecolari sono in uno stato poco eccitato (ground state)
e quindi sufficientemente stabili da fornire il segnale dello ione corrispondente (m/z 122)
nello spettro di massa. Con unenergia compresa nell'intervallo 12,7-15.7 eV gli ioni
molecolari risultano vibrazionalmente eccitati; la rimozione di un elettrone da un orbitale
molecolare ha modificato le frequenze delle vibrazioni dei legami ed anche le forze di
legame nelle diverse parti dello ione.
Fig. 88 - Distribuzione dellenergia degli ioni molecolari
Gli ioni molecolari perdono il frammento neutro .OH e danno il segnale dello ione
corrispondente (m/z 105) nello spettro di massa. Con unenergia superiore ai 15,7 eV gli
ioni molecolari eccitati perdono anche il frammento neutro CO e danno il segnale dello ione
corrispondente (m/z 77). Lo spettro di massa dellacido benzoico riprodotto nella Fig. 89.
78
Spettrometria di massa
Fig. 89 - Spettro di massa dell'acido benzoico
Essendo lenergia vibrazionale superiore allenergia di dissociazione, uno ione comincia a
vibrare e si rompe il legame su cui concentrata la maggior parte di energia. La vibrazione
pi rapida di una molecola organica avviene in 10-13 secondi, cio circa 1000 volte
superiore al tempo impiegato da un elettrone ad alta energia ad attraversare una molecola
organica di alcuni , pari a circa 10-16 secondi. La interazione elettrone-molecola e la
ionizzazione sono talmente rapide che gli ioni molecolari eccitati che si formano non
modificano le lunghezze di legame o le distanze internucleari. Nel tempo immediatamente
successivo, compreso tra 10-16-10-12 secondi, lenergia trasmessa dallelettrone e localizzata
in un punto viene ridistribuita tra tutti i legami, portando ad un equilibrio interno
delleccesso di energia. Questa interpretazione, detta teoria del quasi equilibrio, postula
che vi sia una distribuzione energetica in equilibrio tra i diversi stati quantici possibili
degli ioni. Si tratta comunque di un quasi-equilibrio soltanto momentaneo, perch dopo
10-10-10-6 secondi avviene la frammentazione vera e propria. Lelettrone collidente produce
:
a) ioni vibrazionalmente eccitati, dovuti allestrazione dellelettrone legato pi blandamente;
b) ioni elettronicamente eccitati, dovuti allestrazione di un elettrone da un orbitale pi
interno.
Gli ioni elettronicamente eccitati si trasformano in ioni vibrazionalmente eccitati oppure
cedono leccesso di energia di cui sono dotati sottoforma di radiazioni elettromagnetiche.
Nella popolazione di ioni che si formata, quelli con scarsa energia vibrazionale non si
dissociano, mentre quelli con energia vibrazionale elevata si dissociano in modi e con
velocit diverse, ma sempre in modo tale da produrre i frammenti a pi bassa energia. Gli
ioni molecolari, in conclusione, hanno vita media diversa e quindi probabilit diversa di
comparire nello spettro di massa. Il tempo di permanenza di uno ione nella camera di
ionizzazione di circa 10-6 secondi (1 s), mentre il tempo impiegato da uno ione per
percorrere
il
tubo
analizzatore
(dalla
sorgente
al
dinodo
collettore
-5
dellelettromoltiplicatore) di circa 10 secondi (10 s). Indicando con vm la vita media
dello ione molecolare e con M+, m*, e m+ rispettivamente lo ione molecolare, lo ione
metastabile e lo ione frammento, si possono verificare 3 casi:
vm 10-5 s
vm = 10-5-10-6 s
vm 10-6 s
79
M+ arriva al collettore ed visibile nello spettro di massa;
M+ si decompone lungo il percorso e forma m*
M+ si decompone in sorgente e forma m+
G. Bonaga
Gli ioni frammento possono avere unenergia interna sufficientemente elevata per
decomporsi ulteriormente in ioni-frammento di rapporto m/z inferiore e, ad ogni
passaggio, possono verificarsi anche delle reazioni di trasposizione strutturale che
producono ioni di trasposizione, cio ioni con struttura diversa da quella originale.
In sintesi, linterazione elettrone-molecola un processo che prevede le seguenti fasi:
I^ fase:
II^ fase:
III^fase:
ionizzazione,
ridistribuzione interna dellenergia eccedente il potenziale di ionizzazione,
isomerizzazioni interne, accumulo di energia vibrazionale su certi legami;
frammentazione
5.4.2. FRAMMENTI NEUTRI
Per individuare una struttura incognita le particelle neutre che vengono espulse (sebbene
non visibili nello spettro di massa) sono importanti tanto quanto le particelle cariche.
La conoscenza della esatta sequenza che ha dato origine alla coppia ione e particella neutra
si pu ottenere, nella spettrometria di massa che impiega analizzatori magnetici, con lo
studio degli ioni metastabili. Lidentificazione dei frammenti neutri, ottenuta con la certezza
delle transizioni metastabili o con la probabilit dellapproccio matematico, un elemento
di fondamentale importanza ai fini dellinterpretazione degli spettri di massa, anche
perch le molecole neutre e gli ioni primari sono i pezzi di molecola meno modificati
rispetto la struttura originale.
Ad esempio, alla perdita di particelle di 1, 14, 15, 18 e 59 a.m.u. dallo ione molecolare si
possono associare, rispettivamente, le particelle .H, .CH2, .CH3, H2O e .COOCH3, che
indicano la presenza di un atomo di idrogeno labile (aldeidi, ecc.), di un metile o di un
metilene (catene idrocarburiche), di un ossidrile (alcoli) e di un gruppo estere (esteri).
Nellambito della spettrometria di massa di ioni positivi, sono disponibili le tavole dei
principali frammenti neutri che possono essere espulsi dallo ione molecolare. La Tabella 2
riporta i pi importanti.
80
Spettrometria di massa
Tabella 2 - Frammenti neutri espulsi dallo ione molecolare
m/z
GRUPPO ASSOCIABILE
DEDUZIONI STRUTTURALI POSSIBILI
M-1
M-2
H
H2
Aldeidi
-
M - 14
M - 15
M - 16
M - 16
M - 17
M - 17
M - 18
M - 19
M - 20
- CH2 CH3
O
NH2
OH
NH3
H2O
F
HF
da M-3 a M-13: frammenti di massa non attendibile
Serie omologa
Nitrobenzeni, solfossidi
Arilsolfonammidi, carbossiammidi
Alcoli, aldeidi, chetoni, ecc.
Fluoruri
Fluoruri
da M-21 a M-25: frammenti di massa non attendibile
M - 26
M - 27
M - 28
M - 28
M - 29
M - 29
M - 30
M - 30
M - 30
M - 31
M - 32
M - 32
M - 33
M - 33
M - 34
C2H2
HCN
CO
C2H4
C2H5
CHO
C2H6
CH2O
NO
CH3O
CH3OH
S
H2O + CH3
HSH2S
Idrocarburi aromatici
Nitrili aromatici, eterociclici azotati
Chinoni
Esteri etilici aromatici, esteri etilici, n-propil chetoni
Etil chetoni, n-propil benzeni
Eteri metilici aromatici
Nitrobenzeni
Esteri metilici
Esteri metilici
Tioli
Tioli
da M-35 a M-40: frammenti di massa non attendibile
M - 41
M - 42
M - 42
M - 43
M - 43
M - 44
M - 44
M - 45
M - 45
M - 46
M - 46
M - 48
C3H5
CH2CO
C3H6
C3H7
CH3CO
CO2
C3H8
COOH
C2H5O
C2H5OH
NO2
SO
Esteri propilici
Metil chetoni, acetati aromatici, acetilammine aromatiche
n- e iso-butil chetoni, propileteri aromatici, n-butilbenzeni
Propil chetoni, n-butilbenzeni
Metil chetoni
Anidridi, esteri (riarrangiamento dello scheletro)
Acidi carbossilici
Esteri etilici
Esteri etilici
Nitrobenzeni
Solfossidi aromatici
da M-49 a M-54: frammenti di massa non attendibile
M - 55
M - 56
M - 57
M - 57
M - 58
M - 59
M - 60
81
C4H7
C4H8
C4H9
C2H5CO
C4H10
CH3COO
CH3COOH
Esteri butilici
n- e isoamilbenzeni, n- e iso-butossibenzeni, amil chetoni
Butil chetoni
Etil chetoni
Esteri
Acetati
G. Bonaga
Vi sono alcuni intervalli di massa privi di frammenti: 3-13, 21-25, 35-40 e 49-54, proprio
perch i frammenti neutri la cui massa compresa in questi intervalli non sono attendibili.
La Tabella 3, invece, riporta alcune serie significative di frammenti neutri.
Tabella 3 - Serie di frammenti neutri espulsi dallo ione molecolare
MASSE
FORMULA
DEDUZIONI STRUTTURALI POSSIBILI
1 15 29 43
CnH2n+1
Alcani ramificati
15 31 59
CH3, CH3O, COOCH3
Esteri metilici
1 29 43
H, CHO, CH2CHO
Aldeidi
28 42 56
CO, CH2CO, 2CO
Chetoni ciclici
18 36 46
H2O, 2H2O, H2O+C2H4
Alcoli primari
16 44
NH2, CONH2
Ammidi
16 30 44
O, NO, NO2
Nitroderivati
1 17 45
H, OH, COOH
Acidi carbossilici
19 33 50
F, CH2F, CF2
Organofluorurati
35 36 63
Cl,
32 33 47
HCl, CH2CH2Cl
Cloroderivati
S, HS, CH3S.
Solfoderivati
5.4.3. FRAMMENTI CARICHI
Le serie di frammenti neutri trovano corrispondenza, spesso la conferma, nelle serie di
frammenti carichi, cio quelli formati da ioni ad elettroni pari e quasi sempre a massa
dispari (ad eccezione degli ioni contenenti 1 atomo o un numero dispari di atomi di azoto)
che si collocano nella parte delle masse basse dello spettro. La Tabella 4 riporta alcune
serie significative di frammenti carichi.
Tabella 4 - Serie di frammenti carichi
m/z
FORMULA
DEDUZIONI STRUTTURALI POSSIBILI
15 29 43 57 71 85 99 113
CnH2n+1
Alcani
27 41 55 69 83 97 111
CnH2n-1
Alcheni, cicloalcani
39 53 67 81 95 109
CnH2n-3
Alchini, dieni
30 44 58 72 86 100
CnH2n+2 N
Ammine alifatiche
44 58 72 86 100
CnH2n+2NCO
Ammidi, urea
31 45 59 73 87 101
CnH2n+1O
Alcoli, eteri
29 43 57 71 85 99
CnH2n+1CO
Composti carbonilici saturi
61 75 89 103 117
CnH2n+1O2
Esteri carbossilici
63 77 91 105 119 133
C6H5CnH2n
Fenilalchili
45 59 73 87 101
CnH2n-1S
Tiocicloalcani
105 119 133
C6H4COCnH2n+1
Benzoili
82
Spettrometria di massa
La Tabella 5 riporta gli ioni frammento pi comuni presenti nella zona bassa e media degli
spettri di massa, dai quali se di abbondanza relativa medio alta - si ottengono delle
importanti informazioni strutturali.
Tabella 5 - Ioni frammento pi comuni
m/z
15
18
26
27
28
29
30
31
36/38 (3:1)
39
40
41
42
43
43
44
44
44
44
45
47
49/51(3:1)
50
51
55
56
57
57
58
58
59
59
59
59
60
61
61
66
68
69
69
70
71
83
FORMULA
DEDUZIONI STRUTTURALI POSSIBILI
CH3 +
H2O +
19 25 ioni frammento di massa non significativa
C2H2+
C2H3 +
CO +, C2H4+, N2+
+
+
CHO , C2H5
CH2=NH2 +
ammine primarie ?
CH2=OH +
alcol primari ?
32 35 ioni frammento di massa non significativa
HCl +
+
C3H3
Ar +, C2H4 +
C2H5 +
C2H2O+, C3H6 +
CH3 CO +
CH3 COX
C3H7+
C3H7X
+
C2H6 N
alcune ammine alifatiche
O=C=NH2
ammidi primarie
CO2 + ,C3H8 +
CH2=CH(OH) +
alcune aldeidi
CH2=OCH3 + CH3CH=OH +
alcuni eteri e alcol
46 ione frammento di massa non significativa
CH2 =SH +
tioli alifatici
CH2Cl +
C4H2 +
composti aromatici
C4H3 +
C6H5 X
52-54 ioni frammento di massa non significativa
C4H7+
C4H8 +
C4H9 +
C4H9 X
C2H5CO +
etil chetone, esteri dellacido propionico
CH2=C(OH) CH3+
alcuni metil chetoni, alcuni dialchil chetoni
C3H8N +
alcune ammine alifatiche
COOCH3 +
esteri metilici
CH2 =C(OH)NH2 +
alcune ammidi primarie
C2H5CH=OH +
C2H5CH(OH)-X
CH2=O-C2H5 +
alcuni eteri
CH2=C(OH)OH +
alcuni acidi carbossilici
CH2CH2SH +
tioli alifatici
CH3 CO(OH2 ) +
CH3 COOCnH2n+1
62-65 ioni frammento di massa non significativa
H2S2 +
dialchil disolfuri
CH2CH2CH2CN +
+
CF3
C5H9 +
C5H10 +
C5H11 +
C5H11X
G. Bonaga
71
72
72
73
73
73
74
75
75
76
77
78
79
79/81 (1:1)
80/82 (1:1)
C3H7 CO +
CH2=C(OH) C2H5 +
C3H7 CH=NH2+
C4H9 O +
COOC2H5 +
(CH3)3Si +
CH2=C(OH)OCH3
(CH3)3Si=OH +
C2H5 CO(OH2 ) +
C6H4 +
C6H5 +
C6H6 +
C6H7 +
Br +
HBr +
80
C5H6N +
81
C5H5O +
83/85/87
85
85
CHCl2 +
C6H13 +
C4H9 CO +
85
propil chetone, esteri dellacido butirrico
alcuni etil alchil chetoni
alcune ammine
esteri etilici
(CH3)3SiX
alcuni esteri metilici
(CH3)3SiOX
C2H5 COOCnH2n+1
C6H5X, XC6H4Y
C6H5X
C6H5X
C6H5X
CH2X
N
CH2 X
H
CH2X
O
CHCl3
C6H13X
C4H9 COX
O
85
X
86
86
CH2=C(OH) C3H7 +
C4H9 CH=NH2 +
alcuni propil alchil chetoni
alcune ammine
87
91
92
92
CH2
OH
CH C OCH3
C7H7 +
C7H8 +
XCH2CH2COOCH3
C6H5 CH2X
C6H5 CH2 alchil
C6H6 N +
CH2X
N
91/93 (3:1)
n-alchil cloruri (> esil)
Cl
93/95 (1:1)
94
CH2Br +
C
95
95
C6H7O +
97
C5H5S +
H3C
CH2X
O
CH2X
S
84
Spettrometria di massa
99
99
105
105
C6H5CO +
C8H9 +
106
C7H8N +
107
C7H7O +
107/109 (1:1)
111
C2H4Br +
C6H5COX
CH3-C6H4CH2X
CH2X
H3C
N
CH2X
HO
C O X
C O
S
121
C8H9O +
122
123
127
128
C6H5COOH +
C6H5COOH +
I+
HI +
135/137 (1:1)
CH2X
CH3O
alchil benzoati
n-alchil bromuri
Br
+
130
C9H8N +
141
CH2I +
+
(CH3)2Si O Si(CH3)3
CH2X
N
H
147
O
C
149
OH
dialchil ftalati
C
O
160
C10H10NO +
CH3O
CH2X
N
H
CH3O
190
C11H12NO2 +
CH2X
CH3O
85
N
H
G. Bonaga
ESEMPIO A: n-nonano (mol wt = 128)
La catena idrocarburica paraffinica produce una serie di frammenti carichi e una serie di
frammenti neutri, complementari tra loro:
CH3
15
29
CH2
CH2
43
57
CH2
CH2
71
85
CH2
CH2
99
113
CH2
CH3
128
serie di frammenti carichi: m/z 15, 29, 43, 57, 71, 85, 99, 113
serie di frammenti neutri:
113, 99, 85, 71, 57, 43, 29, 15
Questa serie ad elettroni pari non , in pratica, di grande utilit perch una semplice
ramificazione della catena o qualsiasi altra complicazione strutturale modifica
profondamente la serie di frammenti carichi che si formano.
ESEMPIO B: 1-nonene (mol wt = 126)
La catena idrocarburica olefinica produce una serie di frammenti carichi e una serie di
frammenti neutri, complementari tra loro:
27
CH
CH2
CH2
41
55
CH2
CH2
69
83
CH2
CH2
97
111
CH2
CH3
126
serie di frammenti carichi: m/z 27, 41, 55, 69, 83, 97, 111
serie di frammenti neutri:
99, 85, 71, 57, 43, 29, 15
Anche questa serie ad elettroni pari non di grande utilit per le stesse ragioni esposte
nellesempio precedente.
ESEMPIO C: 1-nonino (mol wt = 124)
La catena idrocarburica acetilenica produce una serie di frammenti carichi e una serie di
frammenti neutri, complementari tra loro:
C
HC
CH2
39
53
CH2
CH2
67
81
CH2
CH2
95
109
CH2
CH3
124
serie di frammenti carichi: m/z 39, 53, 67, 81, 95, 109
serie di frammenti neutri:
85, 71, 57, 43, 29, 15
Anche questa serie ad elettroni pari non di grande utilit, per le stesse ragioni esposte
negli esempi precedenti.
86
Spettrometria di massa
ESEMPIO D: 1-eptilammina (mol wt = 115)
La frammentazione della catena idrocarburica dellammina produce una serie di frammenti
carichi ad elettroni pari, contenenti latomo dazoto (e pertanto a massa pari), e una serie di
frammenti neutri:
H2 N
CH2
30
44
CH2
CH2
58
72
CH2
CH2
86
100
CH2
CH3
115
serie di frammenti carichi: m/z 30, 44, 58, 72, 86, 100
serie di frammenti neutri:
85, 71, 57, 43, 29, 15
Lo ione a m/z 30 caratteristico delle ammine alifatiche.
ESEMPIO E: n-capronammide (mol wt = 115)
La frammentazione della catena idrocarburica dellammide produce una serie di frammenti
carichi ad elettroni pari, contenenti latomo dazoto (e pertanto a massa pari), e una serie di
frammenti neutri:
NH2
44
C
O
CH2
58
72
CH2
CH2
86
100
CH2
CH3
115
serie di frammenti carichi: m/z 44, 58, 72, 86, 100
serie di frammenti neutri:
71, 57, 43, 29, 15
Lo ione a m/z 44 caratteristico delle ammidi carbossiliche e dellurea.
ESEMPIO F: 1-eptanolo (mol wt = 116)
La frammentazione della catena idrocarburica dellalcol produce una serie di frammenti
carichi ad elettroni pari, contenenti il gruppo funzionale OH, e una serie di frammenti
neutri:
HO
CH2
31
45
CH2
CH2
59
73
CH2
CH2
87
101
CH2
CH3
116
serie di frammenti carichi: m/z 31, 45, 59, 73, 87, 101
serie di frammenti neutri:
85, 71, 57, 43, 29, 15
Lo ione a m/z 45 caratteristico degli alcoli e degli eteri alifatici.
87
G. Bonaga
ESEMPIO G: 1-fenilpentano (mol wt = 148)
La frammentazione della catena idrocarburica dellidrocarburo alchilarilico produce una
serie di frammenti carichi ad elettroni pari, contenenti lanello benzenico, e una serie di
frammenti neutri:
CH2
91
105
CH2
CH2
119
133
CH2
CH3
148
trasposizione
- CH2
- CH2
m/z 63
+
m/z 77
m/z 91
(ione tropilio)
C5H3
- C2H2
C4H3
m/z 51
serie di frammenti carichi: m/z 51, 63, 77, 91, 105, 119, 133
serie di frammenti neutri:
(26), (14), 71, 57, 43, 29, 15
Lo ione a m/z 91 (tropilio) caratteristico dei composti benzilici, esso trova conferma nello
ione a m/z 77 (91 - CH2), a sua volta confermato dagli ioni a m/z 63 (77 - CH2) e a m/z 51
(77 - C2H2).
ESEMPIO H: S-metil-1-tiociclopentano (mol wt = 116)
La frammentazione del tiocicloalcano produce una serie di frammenti carichi ad elettroni
pari, contenenti il gruppo HC-S+ legato a frammenti sempre pi piccoli dellanello, e una
serie di frammenti neutri:
H
59
H
45
H
H
101
S
CH3
116
H
H
H
H
73
87
serie di frammenti carichi: m/z
serie di frammenti neutri:
45, 59, 73, 87, 101,
14, 14, 14, 14, 15
Alcuni ioni-frammento sono tipici di particolari strutture. Per esempio, lo ione a m/z 130
caratteristico degli alcaloidi indolinici, quello a m/z 149 degli ftalati usati come plastificanti,
ecc. Gli ioni con valori m/z caratteristici hanno un ruolo determinante nellinterpretazione
strutturale di numerose sostanze naturali, quali alcaloidi, steroidi e peptidi.
Lidentificazione di alcuni gruppi funzionali e dello scheletro idrocarburico di una
molecola di grande utilit nel procedimento di identificaziomne della sua struttura,
pertanto maggiore il numero di ioni frammento visibili sullo spettro tanto pi agevole
il compito di ricostruire la struttura originaria della molecola intera.
88
Spettrometria di massa
5.4.4. IPOTESI STRUTTURALI
Dopo aver tratto dallo spettro di massa le indicazioni relative al peso molecolare, alla formula
molecolare, alla classificazione della sostanza (dallaspetto generale dello spettro e dal
numero di insaturazioni), allindividuazione di alcuni gruppi funzionali, si pu azzardare
qualche ipotesi sulla struttura della molecola. I valori m/z dei picchi e la loro intensit
sono indici delle caratteristiche strutturali della molecola e possono agevolare la
definizione di uno schema logico di frammentazione della molecola (fragmentation
pattern).
Nel caso di composti noti la spettrometria di massa rappresenta unefficace strumento di
conferma della struttura molecolare, mentre nel caso di composti incogniti i risultati della
spettrometria di massa vanno sovente integrati con quelli che si possono ottenere con le
altre tecniche di identificazione strutturale (IR, 1H-NMR, 13C-NMR, UV-VIS, ecc.).
5.4.5. ASSEGNAZIONE E VERIFICA
Dopo aver tentato lidentificazione strutturale, lo spettro di massa dellanalita va
confrontato con gli spettri di massa riportati dalla letteratura e, in qualche misura,
analoghi.
Esistono library che raccolgono da 80.000 a 230.000 spettri (Eight Peak Index of Mass
Spectra, NIST/EPA/NIH Mass Spectral Library, Mc Lafferty and Stauffers Wiley Registry of
Mass Spectral Data. Oggigiorno, con lausilio del computer, il confronto (in realt lanalisi
comparata dei valori di un algoritmo multifattoriale) dura poche decine di secondi e
fornisce la % di somiglianza dello spettro unknow con un certo numero di spettri
analoghi trovati nella library.
5.4.6. REAZIONI IONICHE
a) Reazioni ioniche e strutture ioniche
La spettrometria di massa basata sulla chimica di specie ioniche e radicaliche con tempi
di vita pari a pochi s, con reazioni inconsuete di trasposizione e con la formazione di ioni
di cui si possono conoscere le composizioni elementari, ma le cui strutture effettive sono
per lo pi sconosciute proprio per la brevit della loro vita media. Nonostante ci,
nellinterpretazione dello spettro utile postulare delle ipotesi strutturali relative agli ioni
che si formano.
b) Previsione di reazioni ioniche
Dopo aver stabilito la rappresentazione formale delle reazioni ioniche, la localizzazione
della carica e individuato il legame pi implicato nella ionizzazione, occorre anche
prevedere, tra tutti quelli possibili, il cammino pi probabile della reazione ionica.
Il criterio :
il cammino pi probabile di frammentazione determinato dalla stabilit dei prodotti che si
formano
Se una sostanza ha pi gruppi funzionali e pu dare luogo a pi processi di
frammentazione tra loro competitivi, quali ioni compariranno nel suo spettro di massa ?
La stabilit dei prodotti carichi e neutri governata da tre fattori principali:
1. Effetto induttivo;
2. Compartecipazione di elettroni vicini;
3. Effetto di risonanza.
89
G. Bonaga
1. Effetto induttivo
Consiste nella cessione o nellacquisto di elettroni rispettivamente da gruppi elettronrepulsori (+I) e da gruppi elettron-attrattori (-I) e comporta la formazione di uno ione carico
positivamente. Si considerino ad esempio, i seguenti casi:
2,2-dimetilbutano (mol wt 86)
CH3
a)
CH3
+
+I
H3C C
CH2 CH3
H3C C
+
+ CH2 CH3
CH3
b)
CH3
CH3
+
H3C C
+ CH2 CH3
CH3
tra le due vie possibili la reazione ionica segue la via b) perch comporta la formazione del
carbocatione terziario pi stabile.
propilcloruro (mol wt 58)
H3C CH2
CH2
-I
+
Cl
H3C CH2
+
CH2 + Cl
metiletiletere (mol wt 74)
H3C CH2 CH2
-I
+
O CH3
+
H3C CH2 CH2 +
O CH3
La formazione dei radicali cloro e metossile nei due processi descritti produce la
autoeliminazione di queste specie chimiche dallo spettro di massa.
2. Compartecipazione di elettroni vicini
Riguarda gli ioni contenenti eteroatomi quali N, O e S uniti al carbonio con un legame
semplice. Si rompe omoliticamente il legame C C () e un elettrone forma un legame
() con lelettrone spaiato delleteroatomo. una reazione ionica energeticamente favorita
perch la rottura di un legame bilanciata dalla formazione di un altro legame.
propilammina (mol wt 59)
+
H3C CH2 CH2 NH2
H3C CH2
H3C CH2 CH2 OH
SH
+
CH2 NH2
ione " immonio "
n-propanolo (mol wt 60)
propantiolo (mol wt 76)
H3C CH2 CH2
H3C CH2
H3C CH2
+
CH2 OH
ione " ossonio "
+
CH2 SH
ione " solfonio "
La stabilit delle specie onio decresce nellordine:
90
Spettrometria di massa
N>S>O>Cl
per effetto di questa stabilit - ovvero della differente probabilit dei cammini di reazione
che producono gli onio - che si possono prevedere quali saranno gli ioni prevalenti.
4. amminopropanolo (mol wt 75)
CH2 OH
+
CH2 OH + CH2 CH2 NH2
m/z 31
+
CH2 NH2 + CH2 CH2 OH
a)
CH2
b)
CH2 NH2
m/z 30
La reazione ionica prevalente la b), tanto che nello spettro del composto lo ione a m/z 30
10 volte pi abbondante di quello a m/z 31.
3. Effetto di risonanza
Uno ione che pu essere rappresentato con pi strutture di risonanza pi stabile.
1-butene (mol wt 56)
a)
+
CH2
CH CH2
CH3
b)
CH2
+
CH + CH2
CH3
CH2
+
CH CH2 +
CH3
Delle due possibili rotture in (vinilica) o in (allilica) rispetto il doppio legame, si
verifica soltanto quella b) perch lo ione allile stabilizzato per risonanza:
CH2
+
CH CH2
CH2
+
CH2 CH
+
CH CH2
CH2
etilbenzene (mol wt 58)
CH3
CH2
CH3 +
+
CH2
+
ione " benzile "
ione " tropilio "
La rottura favorita quella in rispetto il fenile, con formazione dello ione benzile che
traspone a ione tropilio.
propanone (mol wt 58)
CH3
CH3
C O
CH3
+
C O +
+
CH3 C O
ione " acilio "
91
CH3
G. Bonaga
Alla stabilizzazione per risonanza si aggiunge anche laspetto energeticamente favorevole
dovuto alla formazione di un terzo legame tra C e O nello ione acilio ad elettroni pari,
legame che non presente nello ione molecolare.
c) Classificazione delle reazioni ioniche
Sempre sulla base della stabilit dei prodotti di frammentazione e sullanalogia di
comportamento di alcuni composti chimici nelle reazioni ioniche, si cercato di mettere a
punto una classificazione delle reazioni osservate nella spettrometria di massa, in modo da
consentire uninterpretazione logica degli spettri.
La classificazione empirica, parziale e spesso infondata, ma anche molto utile. Le
reazioni ioniche sono di due tipi:
a) di scissione
b) di scissione con trasposizione
a) Reazioni ioniche di scissione
S1
C X
S2
C C C
+ X
C C
S3
S4
C C C C
R
R'
C X
+
C C C +
+
R'
H
R
S5
S6
S7
R'
+
C X + R
H
C Y
C
C
R'
+
C Y + R
+
+
C
C
Rotture multiple
Comportano soltanto le rotture di uno o due legami che determinano la frammentazione
semplice (o scissione o fissione) degli ioni. Verranno prese in esame le sette reazioni
ioniche di frammentazione semplice (S).
S1 = rottura alchilica
una frammentazione primaria con rottura del legame C-C degli alcani se X = alchile,
oppure di legami diversi se X = eteroatomo considerato come sostituente saturo (F, Cl, Br,
I, OH, OR, SH, SR, NH2, NHR, NR2). La rottura produce uno ione frammento a elettroni
pari ed favorita dalle ramificazioni della catena perch consentono la formazione di
carbocationi pi stabili (secondari e terziari).
92
Spettrometria di massa
+
C X
C+ +
S2 = rottura olefinica
una frammentazione secondaria che segue la S1, con formazione di una molecola neutra
olefinica e di un altro ione ad elettroni pari.
C+ +
C C C+
C C
Esempio
H H H
C7H15
C C C Cl
Cl + C7H15
S1
H H H
H H H
C C C+
H H H
cloruro di n-decile
S2
C7H15
H
H
H
+
C +
C C
H
H
H
ione n-ottile
ione n-decile
acetilene
S3 = rottura allilica o benzilica
una frammentazione primaria con rottura del legame in . favorita dalla formazione di
cationi stabilizzati per risonanza (ione allile, ione tropilio).
Esempi
Cl
CH2
Cl
S3
cloruro di benzile
C7H15
C C C Cl
H
cloruro di 2-benzile
ione " tropilio "
ione benzile
H H H
+
CH2
S3
Cl + C7H15
H H H
C C C+
H H H
C7H15
H
ione eptilallile
C C C
+
H
S4 = rottura in alleteroatomo saturo
una frammentazione primaria con X = F, Cl, Br, I, OH, OR, SH, SR, NH2, NHR, NR2.
Viene prodotto un radicale alchilico e uno ione a elettroni pari con la carica
sulleteroatomo (onio).
Esempio
CH3
C4H9 C Br
H
2-bromoesano
93
S4
+
CH3 + C4H9 C Br
H
ione pentilbromonio
G. Bonaga
S5 = rottura in alleteroatomo insaturo
una frammentazione primaria con leteroatomo legato con un doppio legame al
carbonio. Gli ioni che si formano si decompongono ulteriormente secondo lo schema di
frammentazione S2.
Esempio
O
CH3CH2
+
CH3CH2 C O + CH2CH3
ione acilio
S5
CH2CH3
S2
3-butanone
+
CH3CH2 + C O
S6 = rottura di retro Diels-Alder
una frammentazione multipla caratteristica delle sostanze contenenti un doppio legame
in un sistema ciclico. Da uno ione molecolare a elettroni dispari si ottiene un frammento
ionico a elettroni dispari ed una specie neutra olefinica.
Esempio
H3C
H3C
CH3
H3C
S6
CH3
1,2,3,4-tetrametilcicloesene
H3C
+
C
CH3
CH3
2,3-dimetil-1,3-butadiene 2-butene
S7 = rotture multiple
Sono frammentazioni multiple che si verificano sia negli ioni molecolari a elettroni dispari
che negli ioni frammento ad elettroni pari.
Esempio
m/z 91
ione tropilio
S7
S7
S7
cicloesano
+
C2H2 + C5H5
S7
+
C2H2 + C3H3
m/z 65
m/z 39
c) Reazioni ioniche di scissione con trasposizione
Alcune volte gli ioni presenti in uno spettro di massa non presentano pi la sequenza
originale di atomi o di gruppi. Significa che non si sono soltanto rotti dei legami dello ione
molecolare, ma un atomo o dei gruppi di atomi si sono trasferiti dalla loro posizione
originale (trasposizione). Inizialmente questi frammenti rappresentarono un disturbo
nellinterpretazione logica degli spettri di massa, ma dopo averle comprese e classificate,
le trasposizioni sono di aiuto nellelucidazione strutturale. Possono essere cos classificate:
1. trasposizioni di idrogeno (casuali e specifiche)
2. trasposizioni strutturali (di atomi diversi da H o di gruppi)
94
Spettrometria di massa
1. Reazioni ioniche con trasposizione di H
La trasposizione pi facile quella di idrogeno, che richiede 4 condizioni:
1. la formazione di un centro di polarit su un gruppo contenente un eteroatomo, per effetto della
ionizzazione;
2. una posizione dellidrogeno nella molecola che sia stericamente favorevole alla sua migrazione;
3. che si formi uno stato di transizione a 6 membri;
4. che la quantit di energia posseduta dallo ione molecolare non sia sufficiente a scindere un
legame.
Se gli elettroni collidenti sono a bassa energia, la reazione di trasposizione favorita
rispetto quella di scissione. In pratica, la molecola ionizzata dallimpatto con gli elettroni
collidenti a bassa energia ha soltanto un piccolo eccesso di energia, tale da orientarsi verso
un riassestamento intramolecolare che richiede un contributo energetico modesto e che
comporta anche la formazione di nuovi legami e leliminazione di particelle neutre stabili.
Verranno trattate le sette reazioni ioniche di scissione con trasposizione di idrogeno (SH) e
le trasposizioni strutturali (SS).
C X
SH1
(C) n
+ X
C H
SH2
SH3
SH4
H2C
H2C
H
CH2
CH2
CH2
B
C
C
D R
+
a) CnH2n+1-X=CH2
+
b) CnH2n+1-CH=X
X+
C
C
X
CH2
+
+
A
D R
H
+
CnH 2n + HX=CH2
+
CnH 2n + CH 2=X
X+
SH5
SH6
+
R X
+
R X H +
X+
X+
.
C
C
a) in ioni con 2 eteroatomi
SH7 Doppia trasposizione di H
b) rottura
95
G. Bonaga
SH1 = trasposizione alcolica
la reazione di eliminazione di una particella neutra stabile di tipo HX (HF, HCl, HBr,
H2O, ROH, H2S, HCN) per migrazione di un atomo di H sullatomo elettronegativo (X =
F, Cl, Br, OH, OR, SH, CN), con conseguente comparsa di uno ione frammento ad elettroni
dispari. la trasposizione tipica degli alcoli.
H
H C O
( CH2) n
H C+
( CH2) n + H2O
H C
SH1
H C H
+ H
H C O
H
( CH2) n
H C
SH2 = trasposizione di McLafferty
Lidrogeno traspone dal C in , previa formazione di uno stato di transizione a 6 membri.
Se nello ione che si forma c un atomo di H nel C in , si pu avere la trasposizione
consecutiva di McLafferty.
Esempio
H3C
.+
H+
O
H
CH3
C
C
H
H C
C
+
C
C
C
C
H SH2
H
H
H
H H
C
H
2
C
C H
H C
H C
H
H H
H H
m/z 128
m/z 86
4-ottanone
CH2
H +
H
O +
CH2
H SH2
C
H
H3C
CH2
H
m/z 58
SH3 = effetto orto
leliminazione di una molecola neutra a spese di due gruppi funzionali posti in
posizione orto in un anello aromatico o in posizione cis in un doppio legame. Uno dei due
gruppi funzionali fornisce latomo di H trasferibile mentre laltro fornisce la parte
complementare della molecola neutra che viene eliminata.
Esempio 1
O H
SH3
C O
+ CH3
O
salicilato di metile
C
C
O H
C O CH3
+
O
Esempio 2
H
.H
SH3
C O
H
+ CH3
O
C
C
.H
C O CH3
+
O
H
H
C
C
C O
+ CH3
O
C O
+ CH3
O
H
H
C
C
O
+ CH3OH
C O
+
O
C O
+
+ CH3OH
96
Spettrometria di massa
SH4 = trasposizioni secondarie
Sono reazioni che si verificano in ioni ad elettroni dispari che provengono da molecole
contenenti gruppi funzionali saturi.
a) lidrogeno traspone sulleteroatomo (la tendenza massima con un atomo di N), si
elimina una particella neutra e si forma uno ione a elettroni pari.
Esempio a)
H
+
H C
N CH2 CH3
C
H
CH3
O
H
H +
CH2 C O
H C + N CH CH
N CH2 +
2
3
SH4 H C
C
H
3
CH3
CH3
O
etilmetilacetilammina
(radical-ione)
b) lidrogeno traspone sullatomo di C adiacente alleteroatomo, si elimina una particella
neutra e si forma uno ione a elettroni pari.
Esempio b)
H
+
H C CH CH F
2
2
H
fluoruro di propile
(radical-ione)
CH2 CH2 + H +
SH4
CH2
+
F
SH5 = migrazione del centro radicalico
la trasposizione di H in molecole cicliche (cicloesano, cicloesilammina, cicloesanolo, ecc),
con eliminazione di un radicale.
Esempio
Nello spettro il picco pi intenso (m/z 55) si forma per migrazione del centro radicalico.
+
O
C
CH2 CH2
CH2
+
O
+
O
CH2
H
SH5
ciclopentanone
(radical-ione m/z 84)
CH2
CH3
CH2
CH2
CH3
CH2
m/z 55
SH6 = trasposizione in alleteroatomo
leliminazione di una particella neutra insatura, con formazione di uno stato di
transizione a 4 membri. una reazione tipica degli acetilderivati di alcol e ammine.
Esempio
CH3
CH2
+ H
CH2 O
CH2
C
O
radical-ione propilacetato
Esempio
97
SH6
CH3
CH2
+ H
CH O
+
O C CH2
G. Bonaga
SH7 = trasposizione doppia
di tue tipi:
a) si traspongono 2 atomi di idrogeno negli ioni contenenti 2 eteroatomi che fungono da
accettori di H e viene eliminato un radicale. la reazione tipica degli esteri degli acidi
carbossilici, degli esteri dellacido fosforico e dei trimetilsilileteri.
Esempio a)
H
H C H
CH2
O
.+
O
C
CH2
CH2
CH3
SH7
H O
+
O
C
+
CH2
CH2
CH3
CH2
CH2
radical-ione etilbutirrato
b) si traspongono 2 atomi di idrogeno, ma leliminazione del radicale avviene per rottura
del legame CC (doppia trasposizione di McLafferty o rottura ).
Esempio b)
H
H C H
+
O
CH2 H
C C CH2
H
H +
O
CH3
SH7
CH2
CH
+
CH2
CH3
CH2
CH2
radical-ione 3-esanone
2. Reazioni ioniche con trasposizioni strutturali
La migrazione non limitata al solo atomo di idrogeno, perch possono trasporre anche
altri radicali - specialmente nei composti aromatici contenenti eteroatomi - con
riassestamenti interni (skeletal rearrangement) che modificano le strutture originali. Sono
reazioni molto numerose e diverse, difficili da classificare secondo un sistema unitario che
risulti anche utile allinterpretazione spettrale. Conviene fare alcuni esempi:
Esempio 1: trans-stilbene ossido (mol wt 196)
98
Spettrometria di massa
Lo ione a m/z 167 si origina dalla seguente trasposizione strutturale:
Esempio 2: dimetilcarbonato (mol wt 90)
Lo ione molecolare a m/z 90 perde un radicale idrogeno per formare lo ione a elettroni
pari a m/z 89 che, attraverso un intermedio a quattro membri, subisce una trasposizione
strutturale con perdita della molecola neutra di CO2 e formazione dello ione a m/z 45.
Lo ione molecolare a m/z 170 subisce un riassestamento interno con mutamento della
posizione degli atomi di H (hydrogen scrambling), poi avviene lespulsione di C=O con
formazione dello ione a m/z 142 (benzociclo-eptatriene) e successivamente la perdita di
un radicale H forma lo ione a m/z 141 (benzotropilio).
99
G. Bonaga
6. INTERPRETAZIONE DEGLI SPETTRI DI MASSA
Da circa ventanni gli spettrometri di massa sono stati dotati di sistemi computerizzati
forniti anche di collezioni (library) di spettri di massa (quelle attuali contengono fino a
230.000 spettri di massa di composti standard). Lidentificazione che si basa sullo schema
logico di frammentazione della sostanza si definisce logic interpretation, mentre quella
che confronta lo spettro del composto incognito con quelli della libreria si definisce
analogic interpretation. Pi frequentemente linterpretazione analogica degli spettri di
massa avvicina soltanto allidentificazione della struttura del composto, dal momento che
essa si basa sul confronto tra il risultato dellequazione multivettoriale applicata al
composto incognito (comprendente i valori m/z del suo spettro e le rispettive
abbondanze) e i risultati delle equazioni multivettoriali dei composti della libreria.
Esistono library che raccolgono da 80.000 a 230.000 spettri (Eight Peak Index of Mass
Spectra, NIST/EPA/NIH Mass Spectral Library, Mc Lafferty and Stauffers Wiley Registry of
Mass Spectral Data).
Esempio
Lequazione multivettoriale applicata ad uno spettro che fornisce la seguente lista delle
masse (mass list):
m/z 102
%
2
73
55
59
100
55
80
43
30
31
38
pu essere scritta con il seguente algoritmo:
102 x 2/100 + 73 x 55/100 + 59 x 100/100 + 55 x 80/100 + 43 x 30/100 + 31 x 38/100 = 167,87
Per identificare il composto incognito con modalit analogiche il computer cerca tra gli
spettri di massa della libreria quelli i cui algoritmi hanno i valori pi prossimi al valore
calcolato per il composto incognito. Nellesempio, il computer fornirebbe tre (spesso molte
di pi) opzioni, ciascuna delle quali con una somiglianza con il composto incognito
espressa in millesimi.
1. 3-esanolo (168,00) = 999/1000
2. 2-esanolo (167,47) = 997/1000
3. 1-esanolo (166,80) = 994/1000
E intuitivo che il 3-esanolo ha lo spettro pi somigliante a quello del composto unknow;
in molti casi queste somiglianze non consentono di individuare con certezza la struttura
delle sostanze, ma soltanto di fornire delle probabilit che comunque - saranno molto
utili o allinterpretazione logica dello spettro di massa oppure ad indicare la pi idonea
strategia per individuare altri elementi strutturali utili allidentificazione della sostanza
sconosciuta.
100
Spettrometria di massa
7. SPETTROMETRIA DI MASSA TANDEM (MS/MS)
Sono stati gi descritti gli accoppiamenti tra la spettrometria di massa (MS) e il sistema di
separazione per gascromatografia (GC) o per cromatografia liquida (LC). Essi separano i
componenti di una miscela e i singoli componenti entrano nello spettrometro di massa.
La MS/MS un accoppiamento analogo, nel quale il primo stadio - quello della
separazione - realizzato da un altro spettrometro di massa.
Supponiamo di analizzare una miscela di sostanze mediante un metodo di ionizzazione
soft (CI, ESI, MALDI, FAB). Ciascuna sostanza produce delle specie ioniche
caratteristiche, quali gli ioni quasi-molecolari [MH]+. Per rendere lesposizione pi
semplice, assumiamo che ciascuna sostanza abbia un unico peso molecolare. Gli spettri di
massa mostrano i picchi di ciascuna sostanza presente nella miscela. Supponiamo anche di
volere identificare una sostanza presente nella miscela: tutti gli spettri di massa forniscono
il peso molecolare, ma sarebbe utile disporre anche degli ioni frammento, che forniscono
altre importanti informazioni strutturali.
La pi semplice spettrometria di massa tandem combina 2 spettrometri di massa (Fig. 90):
Il primo spettrometro usato per selezionare una singola massa (ione genitore =
precursor) caratteristica di un analita della miscela; gli ioni di massa selezionata
passano attraverso una regione (cella di collisione) nella quale sono attivati per vie
diverse (abitualmente per collisione degli ioni con un gas inerte) in modo da produrre
degli ioni frammento (ioni figlio = product). un processo chiamato attivazione per
collisione (CA = collisional activation) o dissociazione indotta da collisione (CID =
collision-inducted dissociation).
Il secondo spettrometro ha il compito di separare gli ioni frammento in base al loro
rapporto m/z.
Nello spettro di massa ottenuto con MS/MS tandem sono visibili soltanto gli ioni figlio
provenienti da uno ione genitore selezionato, in totale assenza di ioni di background e di
ioni provenienti da altre sostanze.
Fig. 90 MS/MS
101
G. Bonaga
Fig. 91 Q-TOF in modalit MS/MS/MS
1:1000; D of 681.3
snap09 AccMass 3 (Top,2, Ht,5000.0,0.00)
1: TOF MSMS 681.30ES+
NF
(128.11)
E
G
(128.11)
bMax
yMax
681.42(M+H) +
100
682.43
291.21
y2
664.39
262.16
b2
147.13
y
102.07 129.12
E
234.15
204.17
a2
y1
263.16
217.13
100
125
150
175
200
225
292.21
293.19
0
75
420.27
391.21
y3
b3
402.26
250
275
300
325
364.18
350
421.26
374.18
375
683.41
400
425
450
478.25
b4
475
567.37
y4
517.28
500
525
550
575
686.10
663.39
577.35
549.34
600
646.38
625
650
675
686.44
M/z
700
Fig. 92 Q-TOF (MS/MS) di una sequenza peptidica
102
Spettrometria di massa
Fig. 93 Spettro parziale di una sequenza peptidica
103
You might also like
- 537 Nuova Elettronica - Imparare Lelettronica Partendo Da Zero, Vol 1 E 2 ItaDocument765 pages537 Nuova Elettronica - Imparare Lelettronica Partendo Da Zero, Vol 1 E 2 ItaDaniele Lombardini88% (8)
- Riassunti Di Chimica GeneraleDocument28 pagesRiassunti Di Chimica GeneraleGiorgia GiovanelliNo ratings yet
- Lezione 1 - La CosmochimicaDocument2 pagesLezione 1 - La CosmochimicaOProfessore MioProfessoreNo ratings yet
- Autoproduzione Cosmetica - SISTEMATODocument80 pagesAutoproduzione Cosmetica - SISTEMATOemiliana magerusanNo ratings yet
- La Struttura Dell'AtomoDocument58 pagesLa Struttura Dell'AtomoSabrina SabatoNo ratings yet
- Chimie Generala Note de CursDocument50 pagesChimie Generala Note de CursContiu MariusNo ratings yet
- Simulazione Fisica 2017Document8 pagesSimulazione Fisica 2017Skuola.netNo ratings yet
- Determinazione Strutturale Tramite Spettrometria Di MassaDocument19 pagesDeterminazione Strutturale Tramite Spettrometria Di MassaFrank Burgay0% (1)
- 1 Introduz ATOMODocument48 pages1 Introduz ATOMOErnestoMissoNo ratings yet
- Microsoft PowerPoint - 2 Sorgente Ei e Sett MagnDocument30 pagesMicrosoft PowerPoint - 2 Sorgente Ei e Sett Magnmastermv2013No ratings yet
- ChimicaDocument6 pagesChimicaLuigiFioreNo ratings yet
- Chimica - Lezione n2 - Teoria AtomicaDocument33 pagesChimica - Lezione n2 - Teoria AtomicaRiccardinoFuffoloNo ratings yet
- Davide Cieri - Studio Della Vita Media Del Mesone BDocument53 pagesDavide Cieri - Studio Della Vita Media Del Mesone BDavide CieriNo ratings yet
- Enrico Fermi - Atomo - Teoria Elettrica Dell'Atomo (Enciclopedia Treccani) (1930) (30p)Document30 pagesEnrico Fermi - Atomo - Teoria Elettrica Dell'Atomo (Enciclopedia Treccani) (1930) (30p)albert_ferrettiNo ratings yet
- Chimica TDocument4 pagesChimica Tluca cimattiNo ratings yet
- Verifica Di ChimicaDocument20 pagesVerifica Di ChimicaEduardo RomilaNo ratings yet
- Manuale Valvole E Amplificazione Del SuonoDocument100 pagesManuale Valvole E Amplificazione Del SuonoGiorgio BattelliNo ratings yet
- Li02 Scientifico Fisica Esempio 2Document14 pagesLi02 Scientifico Fisica Esempio 2Skuola.netNo ratings yet
- Principi Fisici Di Risonanza Magnetica Originale PDFDocument29 pagesPrincipi Fisici Di Risonanza Magnetica Originale PDFMarioNo ratings yet
- Lezione 3 SB22Document71 pagesLezione 3 SB22Martina PorcuNo ratings yet
- MeccanicaQuantistica 01Document23 pagesMeccanicaQuantistica 01complex77No ratings yet
- Modelli AtomiciDocument5 pagesModelli AtomiciFrancesca Di LeoNo ratings yet
- Lezione 3. Teoria ElettronicaDocument42 pagesLezione 3. Teoria ElettronicaRagne FranciscoNo ratings yet
- MetodiDocument7 pagesMetodiLuisaCurlacciNo ratings yet
- Fisica Del PlasmaDocument10 pagesFisica Del PlasmaWhirl009No ratings yet
- chimica - capitolo 7 e 9Document4 pageschimica - capitolo 7 e 9giovannidifonzo10No ratings yet
- Dispense 2016Document51 pagesDispense 2016Daniel Bogdan DincaNo ratings yet
- 2 Modelli Atomici Classici: 2.1 /dvwuxwwxudlqwhuqdghoo DWRPRDocument71 pages2 Modelli Atomici Classici: 2.1 /dvwuxwwxudlqwhuqdghoo DWRPRBenjamin BlairNo ratings yet
- Imparare L'elettronica Partendo Da ZeroDocument765 pagesImparare L'elettronica Partendo Da ZeroRoberto PalazzoloNo ratings yet
- 4 - Spettrometria Di MassaDocument29 pages4 - Spettrometria Di MassaFilippo FirenzuoliNo ratings yet
- Tecnologia Della Fotorivelazione Basata Su Dispositivi A Semiconduttore - Corpo TesiDocument229 pagesTecnologia Della Fotorivelazione Basata Su Dispositivi A Semiconduttore - Corpo TesiEnrico MolinariNo ratings yet
- 3.2 Spettrometria MALDI-ToFDocument14 pages3.2 Spettrometria MALDI-ToFΗλιάνα ΚαλκατζίκουNo ratings yet
- Onde Elettromagnetiche PDFDocument7 pagesOnde Elettromagnetiche PDFOsteofisioNo ratings yet
- Dispensa 3 Chimica SapienzaDocument43 pagesDispensa 3 Chimica SapienzaLorenzo FerrariNo ratings yet
- Fondamenti Di ChimicaDocument38 pagesFondamenti Di ChimicaLorenzo CalviNo ratings yet
- FISICADocument167 pagesFISICAVeronica CapodiciNo ratings yet
- La Natura Della Luce e Il Modello Atomico Di BohrDocument9 pagesLa Natura Della Luce e Il Modello Atomico Di BohrAlessandro Axl Bellapianta100% (1)
- Dispense Di Principi Di Ingegneria NucleareDocument33 pagesDispense Di Principi Di Ingegneria NucleareCristian GrigoreNo ratings yet
- Esercizi Lezione 1Document2 pagesEsercizi Lezione 1Axl_MasterNo ratings yet
- Metodi Chimico Fisici D'indagine Applicati Ai Sistemi Molecolari e NanostrutturatiDocument12 pagesMetodi Chimico Fisici D'indagine Applicati Ai Sistemi Molecolari e NanostrutturatinazzaNo ratings yet
- Lezione1 - Spettroscopia UV VisDocument51 pagesLezione1 - Spettroscopia UV VisventilabroNo ratings yet
- Teoria Delle StringheDocument23 pagesTeoria Delle StringheTamara Remedios BianconiNo ratings yet
- Equazioni Di MaxwellDocument10 pagesEquazioni Di MaxwellSalvatore CacciapuotiNo ratings yet
- Sist Per Ref SolDocument5 pagesSist Per Ref Solmartasantosegea2No ratings yet
- Capitolo 1. Principi Dell'en. NucleareDocument28 pagesCapitolo 1. Principi Dell'en. NucleareAndrea CostanziNo ratings yet
- RIASSUNTI CHIMICA - Natura Della Luce, Energia Quantizzata, Effetto Fotoelettrico e Fotoni, Il Modello Di Bohr, Modello Ondulatorio Dell'Atomo, Onde StazionarieDocument5 pagesRIASSUNTI CHIMICA - Natura Della Luce, Energia Quantizzata, Effetto Fotoelettrico e Fotoni, Il Modello Di Bohr, Modello Ondulatorio Dell'Atomo, Onde StazionarieSebastianHollandLusentiNo ratings yet
- Lo Spettro ElettromagneticoDocument4 pagesLo Spettro ElettromagneticoGabriele VisentinNo ratings yet
- Chimica NucleareDocument5 pagesChimica NuclearefrouniapNo ratings yet
- Meccanica QuantisticaDocument3 pagesMeccanica QuantisticaIkram LazarNo ratings yet
- (Fai Da Te) - Manuale Valvole E Amplificazione Del SuonoDocument76 pages(Fai Da Te) - Manuale Valvole E Amplificazione Del SuonoMichele AlessandriniNo ratings yet
- Esercizi di fisica: fisica nucleare e fisica della materiaFrom EverandEsercizi di fisica: fisica nucleare e fisica della materiaRating: 5 out of 5 stars5/5 (1)
- Esercizi di fisica per licei: onde, ottica e elettromagnetismoFrom EverandEsercizi di fisica per licei: onde, ottica e elettromagnetismoNo ratings yet
- AmmoniacaDocument32 pagesAmmoniacaOrazio MaffeiNo ratings yet
- Boltzmann Il Genio Del DisordineDocument6 pagesBoltzmann Il Genio Del DisordinegiancarlostabileNo ratings yet
- Probiotici e PrebioticiDocument7 pagesProbiotici e PrebioticiFlexyeNo ratings yet
- SURFAL F1214790 Brenntag SDSDocument8 pagesSURFAL F1214790 Brenntag SDSEnrico MolinoNo ratings yet